
一、什么是主动脉瘤?
主动脉瘤并非真正的“肿瘤”,而是指主动脉壁局部异常扩张(超过正常直径的50%),形成类似“气球样”的膨出。根据部位可分为胸主动脉瘤(升主动脉、降主动脉)和腹主动脉瘤(腹部主动脉段)。它是人体内的“不定时炸弹”,一旦破裂,死亡率高达80%以上。
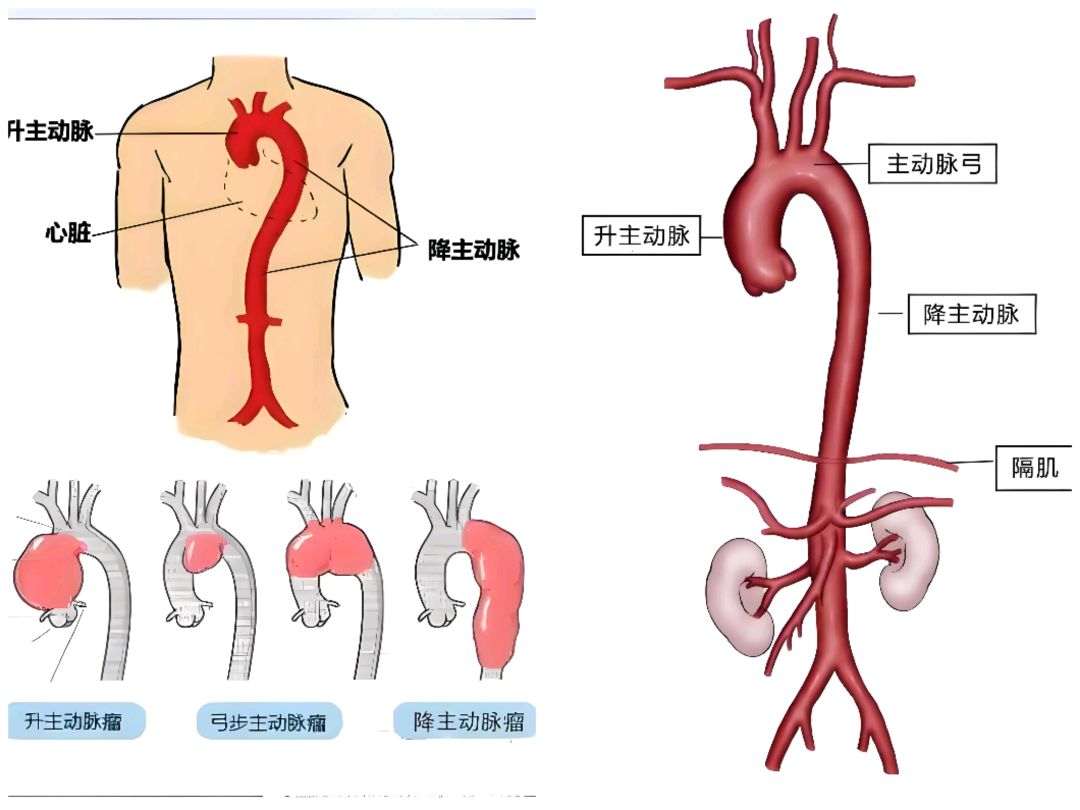
二、主动脉瘤的形成机制
主动脉瘤是主动脉壁异常扩张形成的“血管鼓包”,其形成是多种因素共同作用的结果:
(一)血管壁结构破坏:
1. 动脉粥样硬化:脂质沉积、炎症反应和斑块形成导致血管壁弹性纤维断裂,削弱结构强度,最终在血流冲击下扩张成瘤(占病例的70%以上)。
2. 高血压:长期高压血流冲击血管壁,加速动脉硬化并直接损伤血管中层,形成薄弱点。
3. 遗传因素:马凡综合征、埃勒斯-当洛斯综合征等遗传性疾病因胶原蛋白缺陷,导致主动脉壁脆弱,易形成动脉瘤。
4. 感染与炎症:梅毒、细菌感染引发主动脉炎,破坏血管壁结构;自身免疫性疾病(如红斑狼疮)也可诱发。
5. 分子机制:最新研究发现,TRPM7离子通道激酶通过调控钙、锌离子内流,激活基质金属蛋白酶(如MMP2),导致血管平滑肌细胞凋亡和弹性纤维降解,促进腹主动脉瘤发展。
(二)危险因素:
--不可控因素:高龄(>65岁)、男性(腹主动脉瘤发病率是女性的4倍)、遗传性疾病(如马凡综合征、埃勒斯-当洛斯综合征)。
--可控因素:吸烟(使风险增加5倍)、高血压、动脉粥样硬化、高脂血症。
三、主动脉瘤的危害
1. 破裂风险:瘤体直径≥5.5 cm时破裂风险显著增加,致死率高达80%-90%。破裂后大量失血可在数分钟内导致休克或死亡。
2. 器官压迫:胸主动脉瘤可能压迫气管(呼吸困难)、食道(吞咽困难)或神经(声音嘶哑)。
3. 夹层形成:血流冲击导致血管内膜撕裂,形成夹层,引发剧烈胸背痛、器官缺血(如心肌梗死、肾衰竭)。
4. 继发血栓形成:瘤体内血流缓慢,易形成血栓或继发感染,加重病情。
四、预防:早发现、早干预
1. 控制基础疾病:
- 高血压管理:目标血压≤130/80 mmHg,优先使用β受体阻滞剂(如美托洛尔)降低血管剪切力。
- 降脂治疗:他汀类药物减少斑块形成,延缓动脉硬化。
2. 生活方式干预:
- 戒烟:吸烟者患腹主动脉瘤风险是非吸烟者的5倍以上。
- 饮食调整:低盐、低脂、高纤维饮食,减少饱和脂肪酸摄入。
3. 高危人群筛查:
- 55岁以上男性、有家族史者、长期吸烟或高血压患者,建议定期接受超声或CT血管造影(CTA)检查。
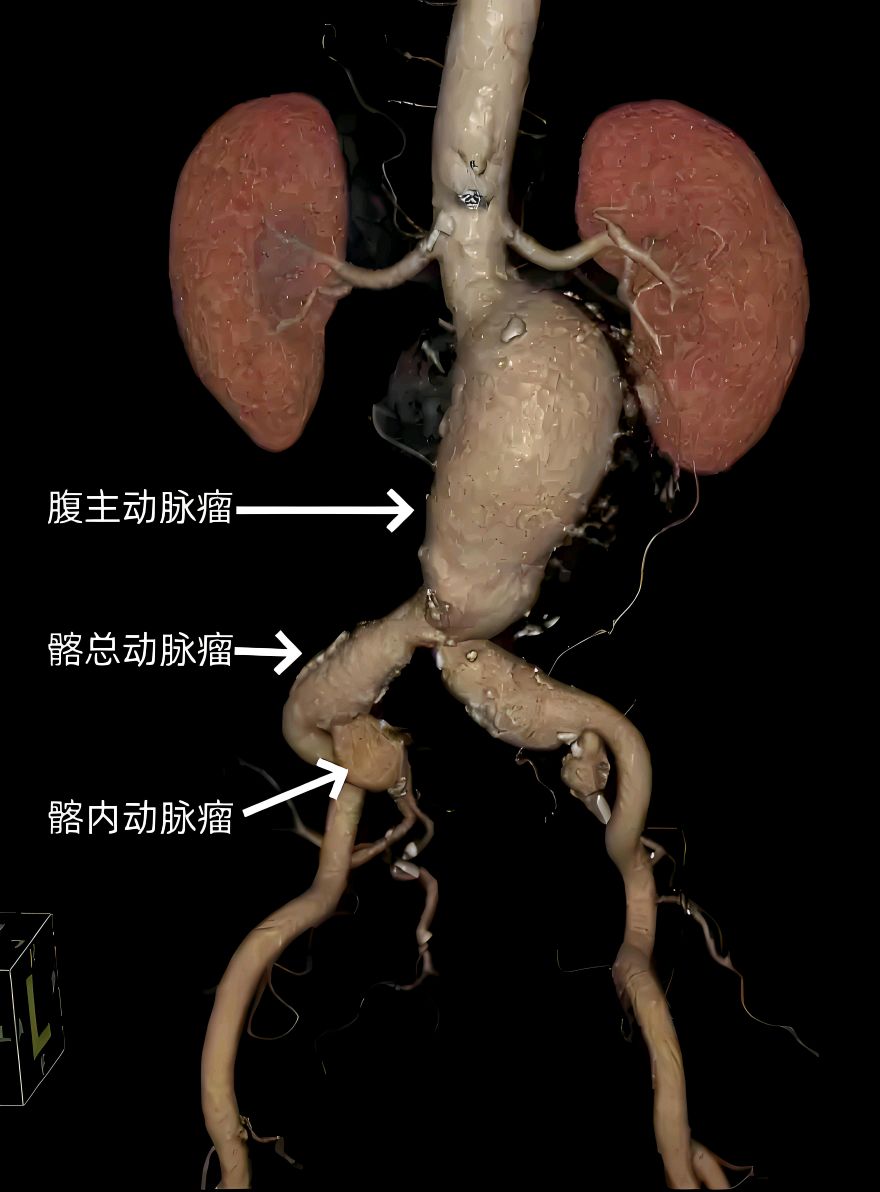
五、诊断与治疗原则
1. 诊断方法:
- 影像学检查:超声用于初筛,CTA为金标准,可精确测量瘤体大小和位置。
- 基因检测:遗传性疾病患者(如马凡综合征)需筛查相关基因突变。
2. 治疗策略:
- 保守治疗:瘤体直径<5 cm时,定期监测(每6-12个月影像复查)+药物控制血压和心率。如:β受体阻滞剂(降低心肌收缩力和血压)、降压药(如ACEI/ARB)。
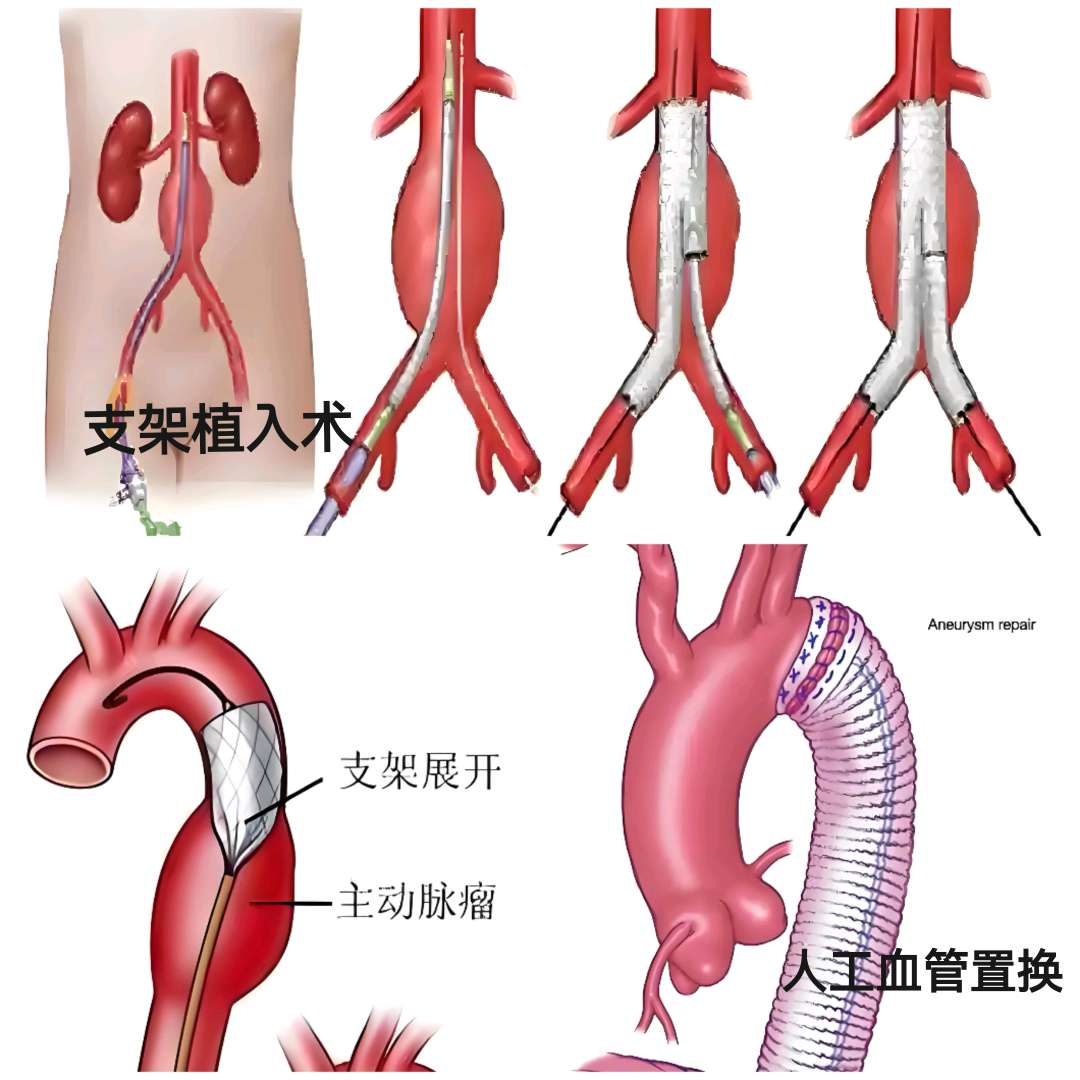
- 手术治疗:
开放手术:传统术式适用于复杂病例,但创伤大、恢复慢; 人工血管置换(适用于年轻、体质较好者)。
腔内修复术(EVAR/TEVAR):微创支架植入,术后次日即可下床,适用于多数主动脉瘤患者。 通过支架隔绝瘤腔(创伤小,适合高龄患者)。
新型技术:烟囱技术(ChEVAR)、分支支架和开窗支架(FEVAR)用于解剖结构复杂的弓部动脉瘤或近肾动脉瘤,长期疗效良好。 另:常温动脉搭桥联合内脏吻合优先策略(NABP)可降低脊髓损伤风险,适用于胸腹主动脉瘤修复。
创新药物:FTY720(芬戈莫德)通过抑制TRPM7通道活性,在动物实验中显著延缓瘤体进展,未来或成新疗法。
六、并发症及预防
1. 术中/术后并发症:
- 内漏:支架周围血流渗入瘤腔,需定期复查CTA,必要时二次干预。
- 器官缺血:支架覆盖分支血管时,可能导致脊髓缺血(严重时可发生截瘫)、内脏器官缺血及臀肌缺血(跛行),需术前精确评估血管解剖。
2. 长期管理:
- 定期随访:术后每年至少一次影像检查,监测支架位置及瘤体变化。
- 感染预防:预防发生支架相关性感染,如及时治疗牙周炎、心内膜炎,糖尿病患者需控制血糖,减少血管感染风险。
结语
主动脉瘤虽非肿瘤,但其破裂致死率极高。通过控制高血压、戒烟、定期筛查,可显著降低发病风险。治疗上,微创腔内手术的普及已大幅提高患者生存率,而TRPM7通道抑制剂等新型疗法的研究为未来提供了希望。早期发现、规范治疗和终身管理是战胜这一“血管炸弹”的关键。