
PRA(Panel Reactive Antibody),即【群体反应性抗体】,是指因输血、妊娠、移植等,机体接触到外源性组织器官HLA抗原,激活免疫系统而产生的【HLA抗体】。如抗体“针对”供者器官,则称为供者特异性抗体(DSA);如“不针对”供者器官,则称为非供者特异性抗体(nDSA)。供者特异性抗体对肾移植的效果影响更大,可导致抗体介导排斥反应(AMR)发生。
在肾移植早期,急性抗体介导排斥反应发生率约1-6%;然而在术前即存在供者特异性抗体的患者,即使接受脱敏治疗,急性抗体介导排斥反应发生率高达21-55%。因此在肾移植术前,移植医师会根据受者PRA的情况,尽量“避开”供者特异性抗体,以达到最好的移植效果,这是配型技术最大的目的。
| 肾移植术后新生DSA的危险因素 |
| 再次移植 |
| 移植前HLA抗体阳性 |
| 年轻(18-35岁) |
| 接受逝者捐献的肾移植 |
| DR、DQ位点错配 |
| 依从性差(自行减药、停药) |
| 免疫抑制强度不足 |
| 炎症(如感染) |
| (亚临床)T细胞介导的排斥反应 |
然而,由于移植肾携带的异体HLA抗原长期刺激机体免疫系统,即使接受免疫抑制治疗,部分患者术后仍可能产生新生供者特异性抗体(de-novo DSA)。上表罗列了肾移植术后新生DSA的高危因素,其中依从性差(自行减药、停药)占最大比重。在肾移植长期随访中,目前研究认为超过60%的移植肾丢失归咎于抗体介导的组织损伤。因此,术后随访中定期监测DSA十分重要。
| 分组 | 定义 | PRA监测策略 |
| 低风险组 | 首次肾移植,移植前未致敏(HLA抗体阴性) | 移植后3至12个月内至少检查一次,此后每年一次 |
| 中风险组 | 移植时无DSA,但曾检出过DSA | 移植后第一个月内,此后至少每年一次 |
| 高风险组 | 移植时DSA阳性 | 除PRA监测外,建议术后3月内进行移植肾穿刺活检 |
注:如有以下情况则随时监测:1、免疫抑制方案改变,2、自行减药、停药、怀疑不依从,3、发生移植肾功能恶化,4、转到偏远中心随访。
按移植时DSA状态将危险度分组,PRA监测策略总结为以上表格。前文提到,肾移植手术时医生会尽量“避开”供者特异性抗体,因此,大部分患者为低风险组或中风险组,每年监测PRA即可。如发现新生DSA且抗体强度较高,推荐行移植肾穿刺活检,以明确是否存在亚临床抗体介导排斥反应(即肾功能正常但已存在病理微观改变,有可能进展为临床典型的抗体介导排斥反应,导致肾功能受损)。如明确亚临床抗体介导排斥反应,应按抗体介导排斥反应进行治疗。
不少患者反映,这个PRA报告我也看不懂啊,全是“验证码”,下面看一个简单的栗子(实际情况多数比这个复杂,还是交给医生看吧
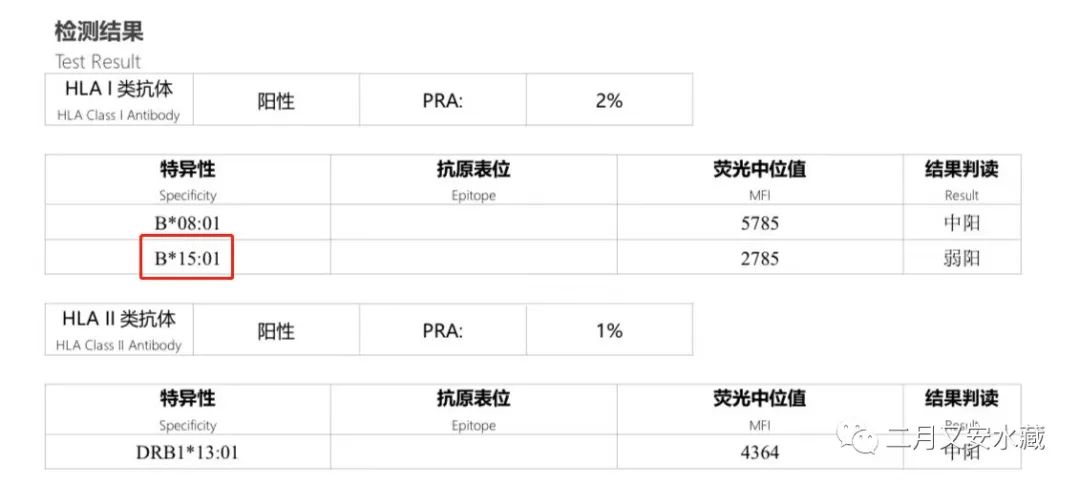
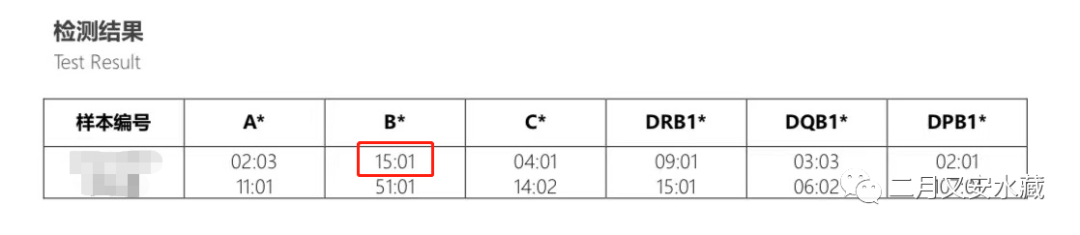
Luminex-immunoassay PRA报告中包含HLA抗体特异性、抗原表位、荧光中位值MFI等信息。简单的理解:【特异性】代表抗体的独特性,是否DSA由它决定;【荧光中位值MFI】代表抗体强度。比如这个受者PRA报告中B*15:01,MFI 2785,判断是否DSA需要比对供者HLA,如供者HLA中同样具有B*15:01这个位点,那么这个B*15:01抗体就是供体特异性的,即DSA。如果这是术前的结果,那么术后急性排斥风险显著升高。如果这是术后新出现的DSA,那么除定期复查外,还建议行移植肾穿刺活检。
随着研究进展,近年还发现MICA、AT1R等【非HLA抗体】,也可引起抗体介导排斥反应。
注:1、本文内容仅供参考,具体诊疗方案请根据自身病情与主管医师沟通制定。2、本文转自本人公众号。