
iNature 2025年07月13日 11:25
肠道菌群及其代谢物与草酸钙(CaOx)肾结石有关,但其确切机制尚不清楚。
2025年6月30日,四川大学王坤杰、金熙共同通讯在Cell Reports(IF=6.9)在线发表题为“Gut microbiota-bile acid crosstalk contributes to calcium oxalate nephropathy through Hsp90α-mediated ferroptosis”的研究论文。该研究强调了肠道菌群-胆汁酸相互作用在CaOx肾结石发病机制中的重要作用。
该研究报道,CaOx肾结石患者的肠道菌群失调会导致脱氧胆酸(DCA)水平升高,而普拉梭菌(F. prausnitzii)的存在减少。DCA与尿液草酸排泄量和结石负担呈正相关,与普拉梭菌丰度呈负相关。给高草酸饮食小鼠补充普拉梭菌可通过减少DCA和次级胆汁酸的产生来减轻肾脏CaOx晶体沉积。DCA抑制肠道草酸分解代谢,通过上调Hsp90α增强CaOx晶体粘附于肾小管上皮细胞,激活Hsp90α/Nrf2/HO-1通路,并通过Hsp90α相互作用和泛素化诱导Gpx4降解,导致亚铁离子积聚、脂质过氧化和铁死亡,从而促进肾脏损伤和CaOx晶体沉积。
肾结石是一种常见的泌尿系统疾病,其患病率从2007-2010年的8.8%上升至2017-2020年的9.9%,美国12个月发病率为2.1%。草酸钙 (CaOx) 是肾结石 (RS) 最常见的成分,约占80%的病例,10年内复发率高达50%以上。CaOx沉积可导致晶体性肾病,这是一种与肾脏炎症、损伤和潜在肾衰竭相关的状态。然而,其具体机制和病理生理学尚未阐明。
最近的研究发现肠道菌群失调与RS之间存在显著关联。与健康个体相比,肾结石患者的肠道菌群多样性降低,组成成分发生改变。然而,大多数研究仅描述CaOx肾结石患者与健康人群相比肠道菌群的紊乱,且仅关注利用草酸的细菌和途径,而忽略了肠道菌群功能的完整性。肠道菌群是一个复杂的生态系统,在人类健康和疾病中发挥着至关重要的作用,并具有巨大的代谢潜力,可以通过各种机制影响宿主的代谢和能量稳态。研究团队之前的研究揭示了肠道菌群衍生的代谢产物短链脂肪酸如何在结石形成过程中调节肾脏的免疫炎症微环境。此外,他们发现另一种肠道菌群代谢产物胆汁酸也在CaOx肾结石的形成中发挥着重要作用。
胆汁酸 (BA) 由肝脏胆固醇合成,通过与肠道菌群相互作用,对调节宿主的代谢和生理至关重要。肠道菌群将原发性胆汁酸(BA)转化为次级BA,改变其信号传导特性并影响宿主代谢。相反,BA通过抗菌活性和激活先天免疫反应来塑造微生物组成。先前的研究提到了高草酸尿症诱发的CaOx肾结石大鼠的BA谱和BA代谢相关途径的改变。然而,具体机制尚未探究。
本研究揭示了CaOx肾结石患者的BA谱和肠道菌群特征的改变。研究发现患者体内Faecalibacterium prausnitzii的减少通过抑制次级BA产生菌及其相关酶活性来降低脱氧胆酸(DCA)水平,从而减轻了高草酸饮食小鼠肾小管CaOx晶体的沉积。从机制上讲,DCA升高会抑制肠道菌群介导的草酸降解,并上调肾小管细胞中Hsp90α的表达。Hsp90α作为CaOx晶体受体,促进晶体细胞粘附,同时通过Gpx4降解和Nrf2/HO-1通路持续激活引发铁超载和脂质过氧化,加剧铁死亡和肾损伤。这些发现凸显了CaOx肾病中肠道菌群-BA相互作用,并提出了以BA代谢为靶点作为肾结石治疗策略的建议。
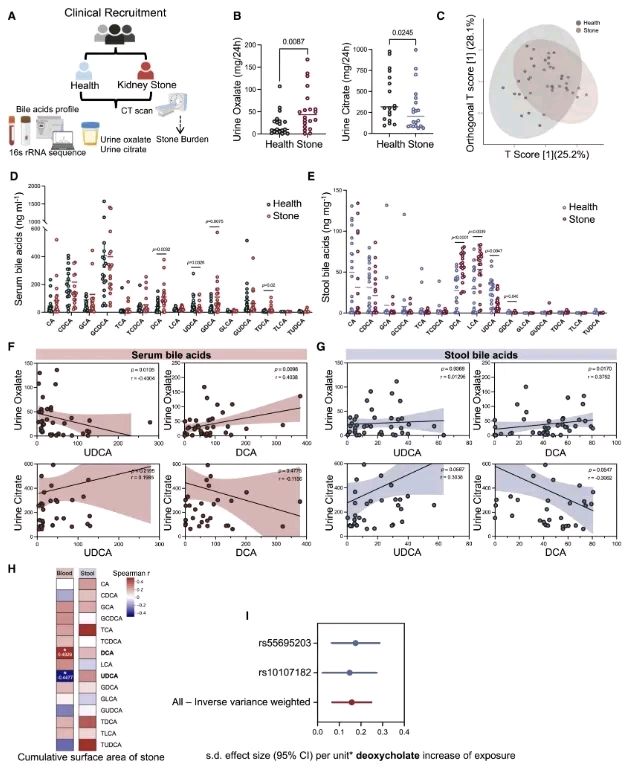
图1 CaOx肾结石患者的胆管菌群失调与结石负担和草酸/柠檬酸排泄有关(图源自Cell Reports)
原文链接:https://www.cell.com/cell-reports/fulltext/S2211-1247(25)00707-7