
医学故事.健康 中华医学会理事 神经外科教授
免疫平衡对机体健康十分重要,过度活跃的促炎状态会导致免疫失调,引起自身免疫性疾病和炎症性疾病[1]。先天免疫和适应性免疫的多种细胞和因子在启动、扩大和终止免疫反应中发挥重要作用[2]。尽管我们知道大脑和外周免疫连接起来的几种潜在途径[3],但作为人体生理学的核心—大脑是如何调节免疫的,目前仍知之甚少。
2024年5月1号,美国哥伦比亚大学Charles S.Zuker教授团队在Nature发表题为"A body–brain circuit that regulates body inflammatory responses"的研究论文,该研究发现一个迷走神经-孤束核的神经回路,确定了环路中对促炎和抗炎免疫介质有反应的迷走神经Trpa1神经元和孤束核Dbh神经元,为大脑调节和塑造机体免疫反应提供了新的观点。

Nature | 调控机体炎症反应的体-脑神经环路
免疫反应通过迷走神经-脑轴激活大脑
首先给小鼠腹腔注射LPS,2小时后促炎和抗炎细胞因子达到峰值,并逐渐下降。c-fos检测发现LPS引起了脑干孤束尾核(cNST)的强烈激活和最后区(AP)区域神经元的激活。cNST是迷走神经传入脑干的主要靶点,是体-脑轴的主要导管。迷走神经的双侧膈下切断后,消除了LPS引起的cNST反应。以上结果表明,外周免疫反应可通过迷走神经-cNST轴激活神经元。

Nature | 调控机体炎症反应的体-脑神经环路
图1 LPS激活cNST神经元
激活cNST神经元抑制炎症
接下来,作者使用活性神经元靶向重组(TRAP)系统将Cre重组酶靶向LPS激活的神经元,利用Cre依赖性iDREADD表达,从而允许化学遗传学靶向抑制或激活。结果显示,化学遗传学抑制cNST神经元导致促炎症反应显著增加,抗炎反应减少。此外,化学遗传学激活cNST神经元则会抑制促炎反应,同时促进抗炎反应。因此,cNST可调控外周免疫反应。
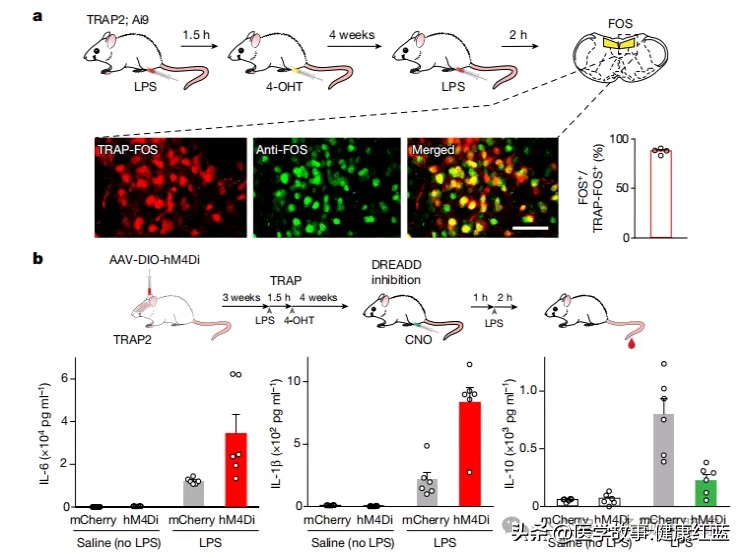
Nature | 调控机体炎症反应的体-脑神经环路
图2 cNST调节炎症反应
cNST脑区中Dbh神经元调节免疫反应
作者对LPS-TRAPed神经元进行scRNA-seq,发现LPS-TRAPed神经元主要存在于3个谷氨酸能簇中(7、10、12)和1个GABA能簇(15)中。进一步分析发现7、10和12群表达多巴胺β-羟化酶(Dbh)基因。脑干中Dbh+神经元几乎完全位于cNST中,并在LPS注射后强烈激活。利用Dbh-cre小鼠进一步证实,cNST中Dbh+神经元的激活显著抑制了促炎细胞因子水平,增加了抗炎因子IL-10水平。消融cNST中的Dbh+神经元则逆转了抗炎表型。因此,以上结果表明Dbh+神经元发挥免疫抑制的能力。

Nature | 调控机体炎症反应的体-脑神经环路
图3 Dbh+神经元调节免疫反应
迷走神经响应免疫细胞因子
作者通过体内钙成像记录迷走神经节中免疫诱发的神经活动,使用单光子功能成像记录迷走神经对腹腔内细胞因子刺激的实时响应。结果显示抗炎和促炎细胞因子激活两个离散的非重叠迷走神经感觉神经元群体。重要的是,LPS并不直接激活迷走神经中的神经元。兴奋性DREADD靶向实验结果表明,激活TRPA1的迷走神经显著增强抗炎反应,同时严重抑制促炎细胞因子的水平。通过靶向表达GCaMP6和使用抗炎或促炎细胞因子激发发现,IL-10而不是促炎细胞因子激活TRPA1迷走神经神经元。以上结果表明,迷走神经的TRPA1+神经元在体-脑轴中传递抗炎症信号,进而增强抗炎状态。
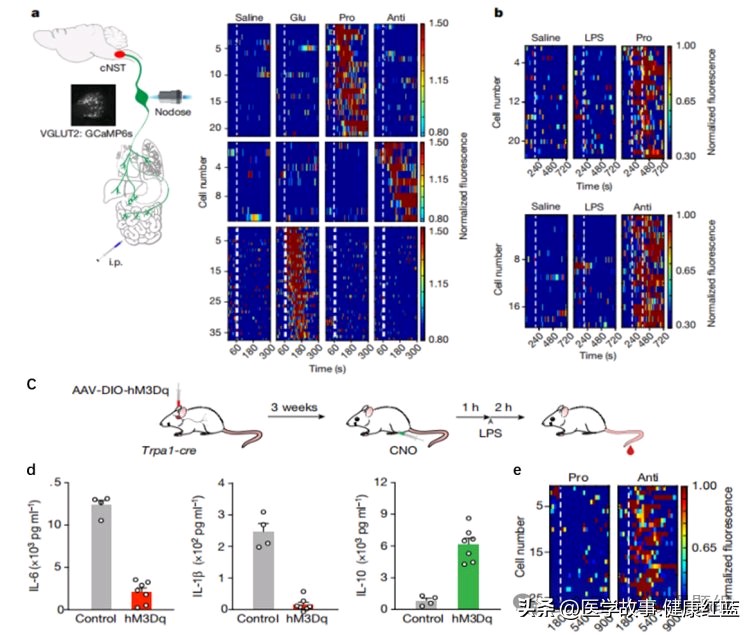
Nature | 调控机体炎症反应的体-脑神经环路
图4 操纵迷走神经元激活可控制炎症
迷走神经-cNST轴维持免疫稳态
cNST的Dbh神经元和迷走神经的Trpa1神经元的激活都可以使LPS致死剂量处理的小鼠存活率显著提高。此外,TRPA1迷走神经神经元的激活抑制了DSS小鼠的炎症表型,炎症因子CXCL1水平和血便评分下降。这表明迷走神经-cNST轴可以维持免疫稳态。
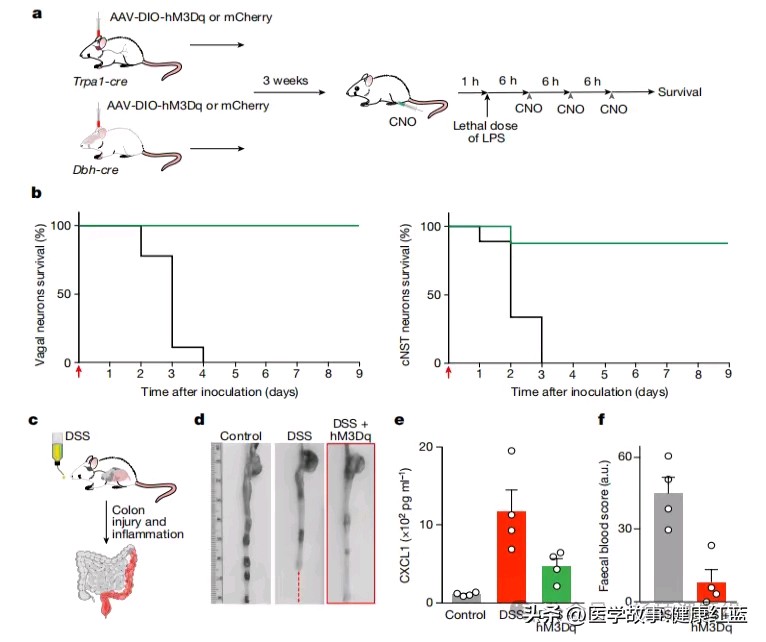
Nature | 调控机体炎症反应的体-脑神经环路
图5 迷走神经-脑轴维持免疫稳态
总结
本研究发现细胞因子本身介导迷走神经-脑的激活,并确定了迷走神经的Trpa1+神经元和cNST的Dbh+神经元可以维持免疫稳态。迷走神经的Calca+神经元响应促炎反应,而Trpa1+神经元响应抗炎信号。迷走神经可以将外周的炎症信息传递给脑干cNST中的神经元,以调控外周的免疫反应。这种体-脑回路可以监测机体炎症反应的发展,并维持促炎和抗炎状态之间的平衡,为靶向神经系统治疗免疫炎症疾病的干预策略开发提供新的思路。
参考文献:
[1] Lee, J. Y. et al. Serum amyloid A proteins induce pathogenic Th17 cells and promote inflammatory disease. Cell 183, 2036–2039 (2020).
[2] Barton, G. M. A calculated response: control of inflammation by the innate immune system. J. Clin. Invest. 118, 413–420 (2008).
[3] Borovikova, L. V. et al. Vagus nerve stimulation attenuates the systemic inflammatory response to endotoxin. Nature 405, 458–462 (2000).