
医学故事.红蓝融合 中华医学会理事 神经外科教授
《自然》新研究,看清DNA损伤修复的过程
研究人员正在研究一种DNA修复途径,即20多年前发现的范可尼贫血(Fanconi anemia, FA)途径。在人的一生中,DNA不断受到环境因素的破坏,包括来自太阳紫外线、饮酒、吸烟、污染和接触化学物质。DNA受损的一种方式是当交联时,它无法正常复制和表达基因。为了自我复制并读取和表达基因,DNA双螺旋的两条链首先必须解压缩成单链。当DNA交联时,两条链的核苷酸粘在一起,阻止解链,包括交联在内的DNA损伤积累会导致癌症。FA通路在人的一生中都很活跃,它能识别这些损伤,并不断修复,基因突变使这一途径不那么有效的个体更容易患癌症。虽然参与FA途径的蛋白质早就被发现了,但它们是如何识别交联DNA并启动DNA修复过程仍然是个谜。以前的研究已经确定了FANCD2-FANCI (D2-I)蛋白复合物,它在FA途径的第一步中起作用,夹在DNA上,从而在交联中启动DNA修复。然而关键问题仍然存在:D2-I如何识别交联DNA?为什么D2-I复合体也与其他类型的DNA损伤有关?这篇文章结合了尖端科学技术,发现D2-I复合物沿着双链DNA滑动,监测其完整性,并且还可视化了它如何识别在哪里停止,允许蛋白质移动,并在那一点上锁定在一起,以启动DNA修复。现代科技为新发现提供了有力的工具。
最近巴黎奥运会正在如火如荼地进行,赛场上,运动员极其迅速的动作、精准而猛烈的发力,让观众目不暇接,甚至是训练有素的裁判有时也无法仅凭肉眼对一些细节做出判断,幸好有高速摄像技术,我们可以一遍遍从多个角度回看、慢放那些精彩瞬间,看清瞬息万变的动态过程。
除了在奥运赛场上,借助尖端的成像技术,在细胞内部,我们现在也能以单分子的分辨率看清生物分子复杂和动态的相互作用过程。
最近,《自然》期刊上线的一篇论文中,来自英国帝国理工学院和剑桥大学MRC分子生物实验室(LMB)的科学家,结合先进的单分子操作工具和可视化工具捕捉到了细胞内至关重要的生物学过程——DNA损伤修复,尤其是DNA修复蛋白如何在单个DNA分子上移动并“锁定”特定位置从而启动DNA修复的。
研究人员指出,这项研究结果解开了有关DNA修复的一个长达数十年的谜团,还为将来更好地治疗癌症带来了新机会。

《自然》新研究,看清DNA损伤修复的过程
DNA分子经常需要修复,因为生命中不断会有环境因素给DNA分子造成损坏,比如阳光中的紫外线、摄入体内的酒精、吸烟、接触到某些污染物,等等。有一类DNA受损方式叫作链间交联(ICL),指的是双螺旋的两条链在某些点“黏”在了一起。在这种情况下,基因的正常复制和表达就会受到阻碍。
不过通常不用担心,因为针对DNA链间交联,细胞有一条专门的修复途径,被称为“范可尼修复途径”(FA途径)。但是,当基因突变导致FA途径无效时,个体就会更容易罹患癌症。还有种名为范可尼贫血症(Fanconi anemia)的人类遗传病就与内源性DNA链接交联的修复缺陷有关。
5

《自然》新研究,看清DNA损伤修复的过程
图片来源:123RF
尽管数十年前科学家就发现了修复DNA损伤的FA途径,还找到了参与FA途径的关键修复蛋白FANCD2-FANCI(简称D2-I),但修复蛋白是怎么识别交联的DNA并启动修复的,这个过程还是不解之谜。
在新研究中,科学家们使用光镊(一种利用光捕获、操控微小物体的工具)捕获了两个微粒之间的单个DNA双链分子,并将其与D2-I蛋白复合体一起孵育。通过单分子成像,研究人员可以记录带荧光标记的单个D2-I蛋白复合体如何在DNA上自由滑动。
I
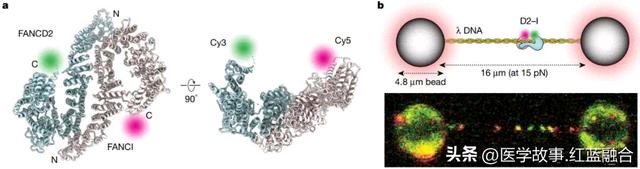
《自然》新研究,看清DNA损伤修复的过程
单分子成像观察带有荧光标记的D2-I在DNA上滑动(图片来源:参考资料[1])
研究人员观察到,钳状的D2-I蛋白并没有直接识别DNA双链中“黏”在一起的交联点,而是始终在自由地双向滑动,直到遇上障碍物“滑不动”了才停止。
时长00:05
用微粒(大圆圈)捕获单个DNA分子(不直接可见),在微粒之间移动的每个红、绿或黄色点都代表一个FANCD2I-FANCI蛋白复合物,它们沿着DNA分子滑动,监测其损伤(视频来源:参考资料[1])
而让D2-I蛋白“卡”住的障碍物就是DNA单链和双链的连接处,是DNA复制时在损伤处形成的。这是因为,DNA在复制时通常需要将两条互补链先解开,并分别在两条单链上形成新的互补链,形成所谓的复制叉。而复制叉在到达DNA链间交联处,由于被黏住的双链无法解开,复制停滞,复制叉的位置产生了暴露的单链间隙。
在这项研究中,科学家们进一步用冷冻电镜解析了D2-I蛋白复合物在打开、关闭和夹紧三种状态下的结构,确认了这些复合物在滑动过程中卡在停滞的复制叉内的单链-双链连接处,并特异性地夹紧该位置。而紧紧锁定在DNA上后,在D2-I蛋白复合物会进一步招募FA修复通路的其他蛋白,启动修复。
时长01:03
FANCD2-FANCI复合体锁定在DNA上准备修复(视频来源:参考资料[1])
研究人员总结说,这些结果表明,触发D2-I复合物停止滑动并夹在DNA上启动修复的原来不是交联的DNA本身,而是由于交联而停滞的复制叉内的DNA结构。由于停滞的复制叉也出现在许多类型DNA损伤中,也就可以解释为什么D2-I复合物在其他形式的DNA修复中也被发现有广泛的作用。
由于DNA损伤是许多疾病的关键因素,同时还是许多化疗药物(例如顺铂)起作用的基础。有些情况下,癌细胞能够抵抗化疗药物,就是因为它们“劫持”了DNA修复途径。正因为如此,通过充分了解DNA修复途径的过程,科学家们有望进一步找到应对癌细胞的方法,开发更有效的癌症药物。
参考资料:
[1] Alcón, P., Kaczmarczyk, A.P., Ray, K.K. et al. FANCD2–FANCI surveys DNA and recognizes double- to single-stranded junctions. Nature (2024). https://doi.org/10.1038/s41586-024-07770-w
[2] Decades long mystery of how DNA damage by sunlight, alcohol and pollution is identified so it can be repaired, is solved. Opens up opportunities for improved cancer treatments. Retrieved Aug. 2, 2024 from https://www.eurekalert.org/news-releases/1053095