
Nat Commun | 中山大学张盛洪团队发现结肠炎潜在的血清生物标志物及治疗靶点
雅涵 iNature 2024年07月17日 09:33 河南 6人听过
iNature
与杯状细胞耗竭有关的粘液损伤是炎症性肠病的早期特征。
2024年7月12日,中山大学张盛洪团队在Nature Communications 在线发表题为“Therapeutic potential of the secreted Kazal-type serine protease inhibitor SPINK4 in colitis”的研究论文,该研究使用单细胞测序检测导致粘液功能障碍的关键因素,发现结肠中Kazal型丝氨酸蛋白酶抑制剂SPINK4与疾病进展同时发生动态变化。化学诱导的炎症性肠病模型中,重组小鼠SPINK4成功改善了特异性敲除Spink4小鼠的疾病状态。值得注意的是,结肠炎治疗中,其与现有的TNF-α抑制剂英夫利昔单抗具有协同治疗作用。
从机制上讲,SPINK4利用Kazal样基序调节EGFR-Wnt/β-连环蛋白和-Hippo通路,促进杯状细胞分化。微生物来源的二酰化脂蛋白Pam2CSK4诱导SPINK4产生。研究还表明,利用非侵入性技术监测循环中的SPINK4可以区分IBD患者和健康人群,并评估疾病发生程度。因此,SPINK4可作为炎症性肠病的血清生物标志物,并具有通过激活影响肠道稳态的内源性EGFR治疗结肠炎的潜力。

炎症性肠病(IBD)主要包括溃疡性结肠炎(UC)和克罗恩病(CD),其特征是分布于整个消化道的慢性和复发性炎症,病因不明。粘液层在空间上将共生微生物群与宿主隔离开来,是内在的第一道防线。近期有研究重点关注炎症性肠病的粘液损伤,并将其定义为溃疡性结肠炎发生和发展过程中的早期特征。葡聚糖硫酸钠(DSS)诱导的结肠炎模型中,由于杯状细胞功能障碍,粘液层在数量和结构上减弱,随后在结肠炎缓解前恢复。
相反,与DSS诱导的小鼠相比,白细胞介素10缺陷型小鼠的结肠粘液层厚度增加,且具备可穿透性。杯状细胞能够在细胞因子、神经递质或微生物群刺激下维持粘液层的完整性,是结肠炎发生的关键影响因素。核心结肠粘蛋白MUC2是形成粘液层所必需的,MUC2敲除小鼠中可观察到自发性肠道炎症。出现胞吐缺陷或MUC2快速降解也是结肠炎易感性增加的早期标志。此外,粘液糖基化或缺乏膳食纤维的粘液溶解微生物群可自行诱发结肠炎,而粘液唾液酸化影响宿主-微生物群的共生稳态。
尽管有上述发现,但仍不清楚结肠杯状细胞(特征为产生粘蛋白)在结肠炎中的作用。随着单细胞RNA测序(scRNA-seq)的出现,部分研究揭示了杯状细胞在靶向先天免疫方面的新功能。前哨杯状细胞产生的粘蛋白具有免疫学特征,包含6个Pyrin结构域的NLR家族(Nlrp6)诱导粘蛋白的产生。炎症性肠病发生过程中出现杯状细胞功能障碍,其产生和分化对于结肠炎的治疗策略的制定越来越重要。尽管表皮生长因子受体(EGFR)、Wnt/β-catenin、Notch和Hippo通路在上皮再生中的重要作用已经得到充分研究,但影响结肠炎粘液恢复的炎症性肠病中杯状细胞分化的研究仍然有限。
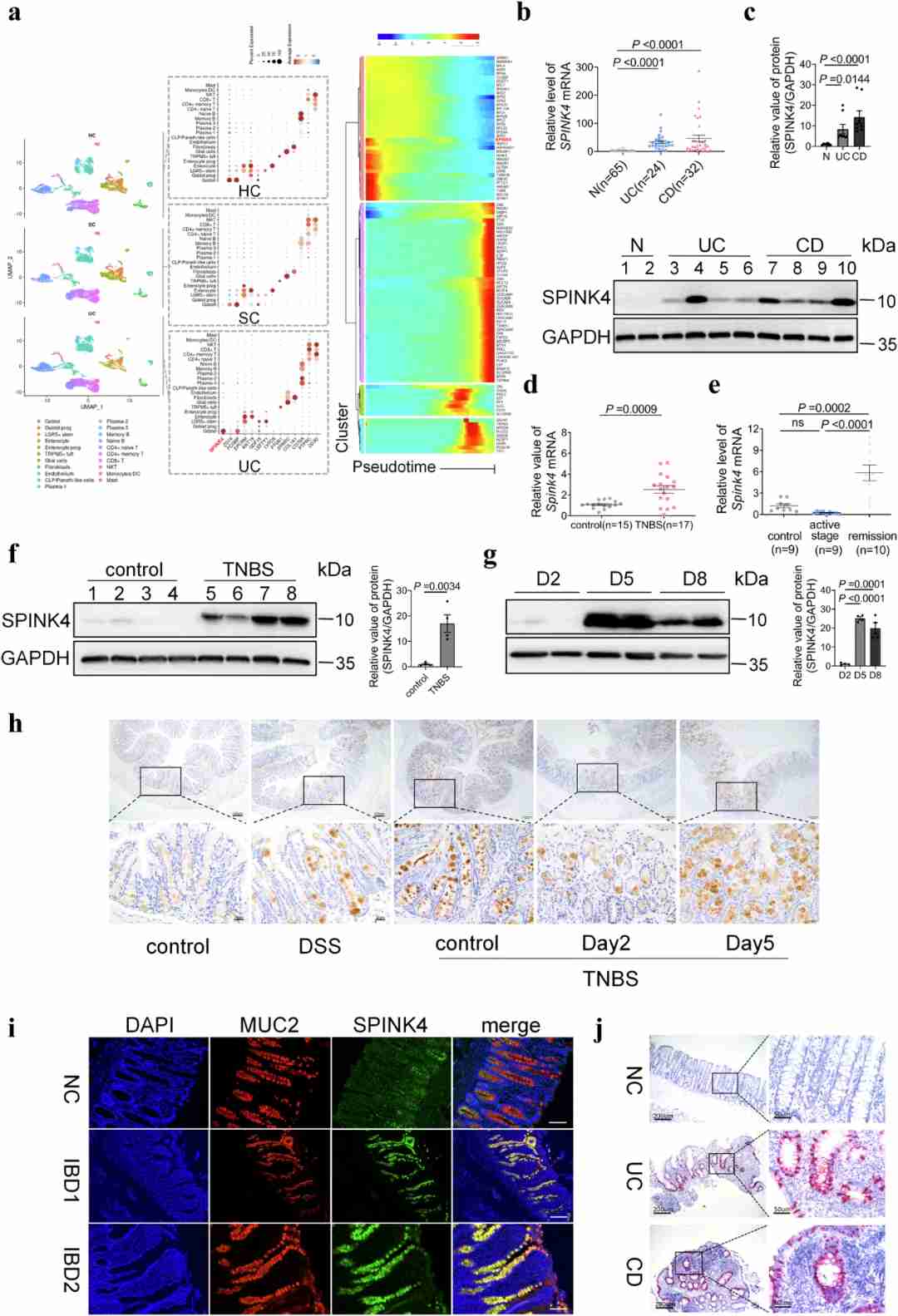
炎症性肠病患者和结肠炎小鼠肠道中SPINK4表达上调(摘自Nature Communications )
为了检测炎症性肠病中粘液功能障碍的关键因素,该团队进行了单细胞分析,发现丝氨酸蛋白酶抑制剂Kazal-type4(SPINK4)(丝氨酸蛋白酶抑制剂家族中一个不为人知的成员)在结肠中出现动态变化。该家族具有与表皮生长因子(EGF)相似的结构,由共享丝氨酸蛋白酶抑制剂Kazal结构域的分泌蛋白组成。SPINK家族中研究最广泛的成员是SPINK1,其导致慢性胰腺炎和癌症的发生。SPINK6参与表皮屏障的修复并促进鼻咽癌的细胞迁移和侵袭。正常情况下,SPINK4在消化道的肠道杯状细胞中少量表达,但仍不清楚其发生机制,很少有关于SPINK4在结直肠癌中作用机制的研究。因此,该研究探索了 SPINK4 在结肠炎中的作用和潜在机制,证明了SPINK4在炎症性肠病中的治疗潜力。
参考消息:
https://www.nature.com/articles/s41467-024-50048-y