
医学顾事
1个月前 · 中华医学会理事 神经外科教授
关注
2022年9月23日,“2023年科学突破奖(The Breakthrough Prize)” 获奖名单公布。美国斯坦福大学的伊曼纽尔·米格诺特(Emmanuel Mignot)和日本筑波大学的柳泽正史(Masashi Yanagisawa)因发现嗜睡症(Narcolepsy)的发病机制获得生命科学大奖。他们的研究工作表明,嗜睡症是因为大脑中缺失了一小群释放促觉醒物质的细胞而引起的,这为开发睡眠障碍治疗的新方法铺平了道路。
文章图片1

生命科学突破奖
(图:breakthroughprize.org)
1、嗜睡症(Narcolepsy)
嗜睡症,又称发作性睡病,是一种慢性睡眠障碍,其核心症状包括难以控制的日间嗜睡、猝倒(Cataplexy)、睡眠瘫痪(Sleep paralysis)以及幻觉(Hallucinations)等。
嗜睡症患者可在没有任何征兆的情况下突然入睡。例如,病人可能在走路或与朋友交谈过程中突然睡着。约70%的嗜睡症患者存在猝倒现象,猝倒是因为肌肉张力突然消失,通常由强烈的正面情绪引起。例如,患者可能在开怀大笑时头部不受控制地下垂或者膝盖突然弯曲。嗜睡症患者在入睡过程中或刚刚醒来时可经历短暂的睡眠瘫痪。睡眠瘫痪是一个非常恐怖的过程,你会发现无法控制自己的身体,无法活动或讲话。睡眠瘫痪也可能伴有幻觉出现。
嗜睡症患者的猝倒、睡眠瘫痪和幻觉等症状与快速眼动睡眠(REM)的异常相关。通常情况下,睡眠周期起始于非快速眼动睡眠(NREM),然后过渡到快速眼动睡眠;而嗜睡症患者在入睡后会很快进入快速眼动睡眠,病人可能在没有完全睡着的时候就开始做梦,这时梦境与现实就会混淆,从而导致幻觉。嗜睡症患者的睡眠周期紊乱还表现在可从觉醒期直接进入快速眼动睡眠期。
2
嗜睡症早期研究
嗜睡症首先由德国医生威斯特法尔(Westphal)和法国医生热利诺(Gélineau)分别于1877和1880年报道。长久以来,人们对该疾病的致病原因并不了解。
1972年斯坦福睡眠研究中心的创始人威廉·德门特(William Dement)在一次科普讲座上展示了嗜睡症病人的发病视频,观众中一位兽医发现该病人的表现与他曾经救治过一只狗的症状非常类似。不幸的是这只狗已经被安乐死,但从留存的视频中还是可以看到狗的症状跟嗜睡症患者的症状非常相似。
德门特敏锐地觉察到,嗜睡症动物可能是研究致病机制的一个突破口。于是,他和同事开始与全美国的兽医取得联系收集嗜睡犬。经过不懈努力,他们于1975年获得了几只患病的杜宾犬,这些杜宾犬于1976年产下嗜睡症幼崽,首次证明了嗜睡症的遗传性。之后在意大利遗传学家卡瓦利-斯福尔扎(Luigi Luca Cavalli-Sforza)的协助下,德门特发现嗜睡症状为常染色体隐性遗传,但是并未找到致病基因。
文章图片2

嗜睡犬(图:参考文献3)
3
嗜睡症致病基因
受到上述工作的启发,米格诺特(Emmanuel Mignot)决定克隆嗜睡症的致病基因。然而在1980年代,这样的工作需要巨大的勇气,因为当时人类基因组计划等大规模测序活动尚未完成,只能采用原位克隆等一些低效率的技术手段。在一次采访中,米格诺特教授说“当时大家都认为我的想法很疯狂。我承认这确实太疯狂了,花费了我10 年时间,但是最终我认为这一切都是值得的”。
克隆嗜睡症致病基因的进展并不顺利,直到研究者发现狗的12号染色体跟人类6号染色体存在大片段同源,这样他们就可以利用人类基因组测序的一些初步数据,这是整个工作的转折点。最终米格诺特成功锁定包含两个潜在基因的片段,并发现其中的下丘脑泌素二型受体基因(Hypocretin receptor 2,HCRTR2)的突变是导致拉布拉多和杜宾犬嗜睡症的原因。这一工作于1998年在Cell杂志发表。
文章图片3

Emmanuel Mignot 和一只患有嗜睡症的狗。Mignot教授现任斯坦福睡眠研究中心主任(继任于William Dement)(图:Lenny Gonzalez)
4
发现下丘脑泌素食欲素系统
正当斯坦福睡眠研究中心的科学家们如火如荼的研究犬类嗜睡症致病机制的时候,斯克里普斯研究所(Scripps Research Institute)的另一组科学家正在寻找下丘脑特异的基因。路易斯·德莱西亚(Luis De Lecea)和托马斯·基尔达夫(Thomas Kilduff)等1998年在美国科学院院刊(PNAS)上报道了下丘脑特异神经肽—下丘脑泌素(Hypocretin,Hcrt),该基因编码了I型(HCRT1)和II型(HCRT2)下丘脑泌素前体。巧合的是,该工作发表后一个月,西南医学中心(University of Texas Southwestern Medical Center)的日本科学家樱井武(Takeshi Sakurai)和柳泽正史(Masashi Yanagisawa)在Cell杂志也发表了一项工作,报道了他们发现两种神经肽—食欲素A和B(OrexinAB)以及对应的食欲素受体,其中食欲素与德莱西亚等人发现的下丘脑泌素为同一物质,而其中的II型食欲素受体也就是导致犬类嗜睡症的基因。
值得一提的是,樱井武的发现完全独立于德莱西亚的工作,他们工作的初衷是寻找孤儿受体(Orphan GPCRs)的内源配体。孤儿受体是指根据基因序列的同源性确定的一组GPCR,但是尚未找到它们的内源配体。鉴于孤儿受体可能为潜在的药物靶点,相关研究一直是领域内一大热点。樱井武等人首先把孤儿受体表达在细胞系中,然后施加脑提取物,当提取物与孤儿受体结合引起下游反应时,进一步采用高效液相色谱鉴定提取物的有效成分。通过上述实验,他们发现了孤儿受体HFGAN72(也就是I型食欲素受体)的内源配体并命名为食欲素,进一步他们发现食欲素基因特异在外侧下丘脑表达,可调控小鼠的进食行为。
德莱西亚和樱井武工作的初衷并不是寻找嗜睡症的致病基因,而是希望通过调控外侧下丘脑的神经活动来控制肥胖。实际上以上两位作者在1998年分别发表的文章中,均暗示下丘脑泌素食欲素系统在饮食调控中的作用。之后,柳泽正史实验室进一步制备了食欲素基因缺失的小鼠,但是他们并未发现突变小鼠的进食行为发生明显改变,不过有意思的是研究者发现该小鼠经常突然停止运动,疑似嗜睡症的猝倒。进一步采用脑电记录,研究者发现突变小鼠猝倒是因为从觉醒状态直接进入快速眼动睡眠。这一发现进一步确认食欲素系统的缺失为嗜睡症的致病原因。
文章图片4

Masashi Yanagisawa 现任筑波大学世界睡眠研究所所长
(图:wpi-iiis.tsukuba.ac.jp)
5
嗜睡症与自身免疫
故事到这里并没有结束。虽然早期研究提示嗜睡症具有家族遗传特征,并且在小鼠和犬类上的基因研究也证明下丘脑泌素食欲素系统的功能缺失可导致嗜睡症。但是,更多研究表明人类嗜睡症通常并不具有遗传性,并且很多嗜睡症患者也没有相应的基因突变,提示环境因素的重要性。
后续研究发现,嗜睡症患者血清中下丘脑泌素食欲素浓度大幅度降低,表明病人下丘脑中这些神经元被损伤,之后采用患者脑组织进行的原位检测也证实了这一猜测。目前认为,人类嗜睡症主要由自身免疫反应引起,患者免疫功能出现异常,攻击自身组织,导致下丘脑泌素食欲素神经元死亡。这一假说也与早期遗传学研究一致,遗传筛选发现调节免疫反应的人类白细胞抗原特定亚型(HLA-DQ0602)与嗜睡症高度相关。
文章图片5
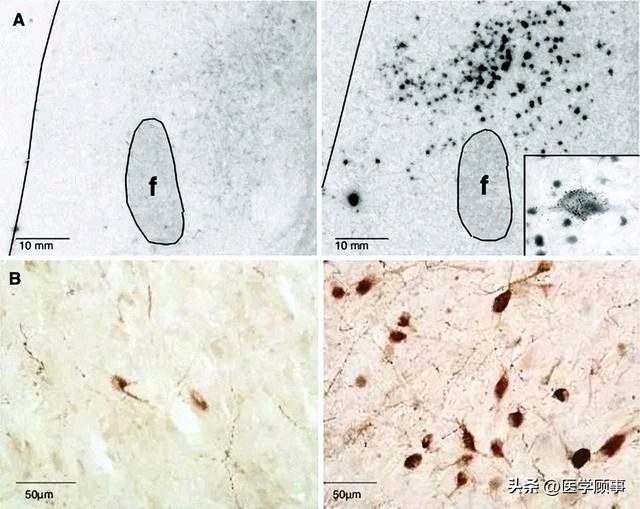
嗜睡症患者脑组织(左)下丘脑泌素食欲素神经元死亡(图:参考文献3)
另一方面,由中国学者主导的一项研究也进一步支持了嗜睡症的自身免疫起源假说。北医六院韩芳教授长期接诊嗜睡症患者,其中70%的患者为儿童,并且这些儿童的发病呈现出极强的季节性,绝大多数病例集中在春季,这极有可能是由季节性上呼吸道感染所触发。更有意思的是,随着2009年H1N1禽流感大流行,嗜睡症患者的数量也大幅增加。后续研究发现2009-H1N1病毒含有下丘脑泌素食欲素相似序列,这可能是导致免疫系统错误杀伤自身细胞的原因。
6
嗜睡症临床治疗
嗜睡症作为一种慢性疾病,目前主要通过药物治疗。常用的临床药物包括哌甲酯(Methylphenidate)和莫达非尼(Modafinil),二者均为中枢神经系统兴奋剂,主要通过上调脑内去甲肾上腺素系统和多巴胺系统来达到促觉醒效果
7
下丘脑泌素食欲素系统与睡眠调控
下丘脑泌素食欲素系统的研究也为我们理解睡眠调控机制带来诸多启示。
关于脑内神经活动如何调控睡眠-觉醒周期的转换有多种理论,其中哈佛大学克利福德·萨珀(Clifford Saper)提出了双稳态触发器模型(“flip-flop” model)。该模型中,睡眠与觉醒为相互拮抗的两个稳态,它们分别由促睡眠环路和促觉醒环路控制,这两个环路相互抑制,当促睡眠环路活跃时可抑制促觉醒环路,机体处于睡眠状态;反之则处于觉醒状态。而下丘脑泌素食欲素系统可以稳定睡眠和觉醒这两种状态,该系统功能失常则导致睡眠-觉醒周期转换异常。这一模型可以在一定程度上解释嗜睡症患者睡眠-觉醒行为的异常,包括睡眠碎片化,日间嗜睡以及觉醒到快速眼动睡眠的直接转换等。
此外,利用嗜睡症模型小鼠的最新研究也揭示了快速眼动睡眠调控的新机制。部分嗜睡症患者在经历强烈的正面情绪时会发生猝倒症状,该现象也存在于模型小鼠中,给予模型小鼠喂食巧克力可以快速诱导猝倒症状。樱井武在最新发表的工作中发现,模型小鼠的猝倒症状伴随着杏仁核脑区(Basolateral Amygdala)多巴胺释放的瞬时升高,而这种多巴胺的瞬时上升可导致小鼠进入快速眼动睡眠。该工作揭示了大脑调控快速眼动睡眠的全新机制,有别于传统上认为快速眼动睡眠主要由脑干神经环路调控的概念。
8
下丘脑泌素食欲素系统与失眠治疗
下丘脑泌素食欲素系统是也新一代促睡眠药物的重要靶点。
失眠等睡眠障碍非常普遍,据统计有超过30%的人曾有失眠。慢性失眠对免疫系统、循环系统、代谢系统等带来一系列负面影响,是高血压、糖尿病、阿尔茨海默病(老年痴呆)、以及抑郁症等情绪障碍的重要风险因素。因此,开发高效安全的安眠药物是迫切需求。
传统促眠药物主要通过增强脑内GABA抑制性传递来达到镇静催眠效果,但是这与大脑睡眠时的工作模式并不相同。按照失眠的环路理论,大脑觉醒系统的过度活化是患者难以入睡的重要原因,因此可通过拮抗促觉醒系统来实现促睡眠效果。而下丘脑泌素食欲素系统作为重要的促觉醒系统,是极有潜力的药物靶点。目前,按照上述思路开发的食欲素受体拮抗剂已经应用于临床失眠症的治疗。
9
总结与展望
研究者首先从嗜睡症发病机制入手,揭示了下丘脑泌素食欲素系统在睡眠-觉醒调控中的重要作用,相关研究成果也为睡眠障碍治疗提供了新药物靶点。
虽然我们在嗜睡症致病机制以及下丘脑泌素食欲素系统在睡眠调控中的重要作用等方面已经取得了重大进展,但是还有多个谜团尚未完全解开。例如,免疫系统如何杀伤这些脑内神经元?下丘脑泌素食欲素系统参与睡眠调控的确切机制是什么?这些重要问题都有待于进一步探索。
最后,欢迎对睡眠研究有兴趣的小伙伴们加入我们,共同探索睡眠的奥秘(文末链接有招聘广告,也欢迎实习和毕业设计的同学)。
作者:中科院脑智卓越中心研究员 徐敏
本文来自睡眠奥秘,未经授权不得转载。
如有需要请联系:xulabsleep@outlook.com
参考:
1) https://breakthroughprize.org/News/73
2)https://www.mayoclinic.org/diseases-conditions/narcolepsy/symptoms-causes/syc-20375497
3)https://link.springer.com/article/10.1007/s12026-014-8513-4
4)https://www.newscientist.com/article/2339153-scientists-who-discovered-cause-of-narcolepsy-win-breakthrough-prize/