
一、附睾的解剖
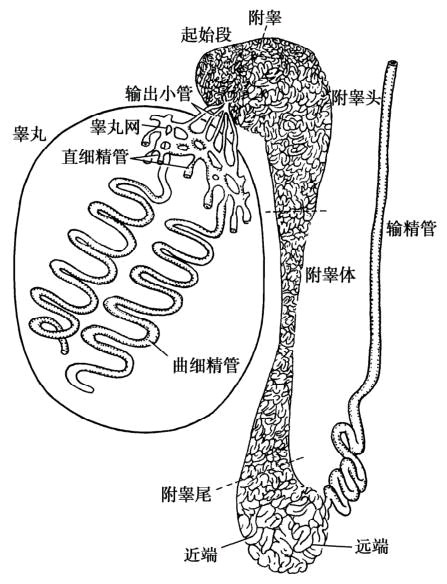
附睾呈新月形,由睾丸输出小管和迂曲的附睾管组成,紧贴睾丸的上端和后缘。上端较为膨大,呈钝圆状,附于睾丸上端的后方,称附睾头;附睾头下行变圆如柱,无明显膨大,称附睾体;至睾丸后下缘渐尖细,借疏松结缔组织与睾丸后缘相连,称附睾尾;附睾尾末端自后方急转直上,移行于输精管。
左右附睾的大小基本一致,成年国人右侧附睾平均长5.29cm,左侧平均长5.18cm。
附睾表面也像睾丸一样,覆盖同样的三层膜,由外而内依次为鞘膜脏层、白膜和血管膜,与睾丸者相连续,但一般稍薄。
附睾实质系由睾丸输出小管及附睾管共同组成。在睾丸纵隔处,输出小管与睾丸网小管相连,该处睾丸网小管首先汇集成8~15条小管,然后穿出睾丸形成输出小管,进入附睾头起始部。输出小管初为直行,随后出现轻度弯曲,愈近附睾小叶底部迂曲愈加显著,在抵达小叶底部后,该类小管由上而下,依次汇集成一条总管,即附睾管,其迂回盘绕,下行构成附睾体。附睾管进一步再下行,管径逐渐增大,至附睾尾处管腔达到最大,最后在附睾尾的末端反转上行,遂移行成为输精管。
尽管附睾仅为一个长约5cm的实质器官,但如将盘区的附睾管展开拉直时,其全长则可达4~6m。关于附睾的分区,一般皆惯于遵循解剖学惯例,但有生殖生物学者依据附睾管的集团性、管径、管壁管腔大小、上皮细胞的组织学特征等,建议做细微分区,把人类附睾分为8区或9带(第1带相当于起始段,2~4带相当于附睾头,5~6带相当于附睾体,7~9带相当于附睾尾)。
在附睾头部,可见富含血管和弹性纤维的结缔组织,伸入附睾实质形成附睾小隔,附睾小隔将附睾头分隔成8~15个小叶,称附睾小叶,每一小叶状如圆锥,长约10mm,故又称附睾圆锥,又因每一小叶多成自一条高度盘曲的睾丸输出小管,所以也可叫输出小管圆锥;小叶底均朝向附睾头的游离缘,而顶尖部则朝向睾丸纵隔;小叶间结缔组织均彼此连续。
附睾头附近常有长圆形突起,借细茎与附睾头相连,有时有分叉,称附睾附件,系胚胎时期中肾管(又称Wolff管)分化发育中遗留的残迹;附睾头上方、精索下端,或输出小管尾侧的结缔组织内,有时出现扁平白色的游离性小体,长约0.5~0.6cm,为一些独立的或群集的囊性小体,称旁睾,亦系胚胎时期中肾尾侧的中肾小管所残留,一般常见于新生儿,6~10岁的儿童最易辨认,成年时已少见。
此外,在附睾头和附睾尾,有时还可见到一些迂曲的退化性小管,一端连通着睾丸网或附睾管,另一端为盲端,其与睾丸网小管相连且位于附睾头前方者称上迷管,系发育不全的输出小管,一般较罕见;其与附睾尾小管相连者,则称下迷管,较长,盲端可达附睾体部,若拉直可达5~35cm。上、下迷管分别是胚胎期头尾侧中肾小管的残留物。至于中肾旁管(又称Müller管)分化发育中,在头端残留所形成的泡状物,则位于睾丸上端附睾头端的结缔组织中,称睾丸囊状附件。
上述这些先天性残余体,通常情况下并不表现任何生理意义,若因某些内、外因素的长期影响,也可能激发其细胞异常增生形成肿瘤。
二、附睾与精子的成熟
精子在睾丸中产生后,从形态结构及染色质角度看已基本成熟,但还不具备运动能力和受精能力,进入附睾后,沿着附睾头、体、尾运行和贮存的过程中,精子会进一步进行变化,形态结构、物质代谢和细胞膜成分都发生改变。精子通过附睾,获得运动能力(与附睾精子运动能力获得和发育的相关因素很多且很复杂。
目前总括起来可以归结为4个方面:
①精子附睾成熟运行过程中的结构变化影响,如精子鞭毛的结构包括巯基的变化;
②附睾精子的能量系统发育,如精子线粒体功能、精子的糖代谢、肉毒碱以及ATP等;
③精子细胞信使系统,如钙离子、钙调蛋白以及cAMP等;
④附睾液中的某些离子成分的影响。这些因素间存在复杂的相互作用关系)和受精能力(受精过程是精卵相互作用最终形成受精卵的复杂过程,包括对透明带的黏附、识别和穿透,精卵识别,精子的穿入和精卵的融合等。
研究表明,精子的受精能力是在附睾运行和贮存过程中获得和发育的,是附睾精子成熟的核心。
附睾精子受精能力获得和发育的研究是Bedford和Orgebin-Crist于1967年首先在兔上进行的。他们采用结扎方法使附睾精子不能循附睾头体尾进行运行,而只能停留在附睾近中段。虽然近中段附睾精子能存活,但却无受精能力。随后上述两位学者和其他科学工作者对狷猴、猪、羊、小鼠、大鼠、田鼠等附睾精子进行了系统研究;在人类也发现大部分附睾精子进入到体尾部的过程中获得了受精能力。而在附睾管阻塞或缺失时,近中段部分的精子仅一小部分具有受精能力。
至此,对包括人在内的附睾精子受精能力获得的部位基本清楚。人类精子在从附睾头部进入到附睾体尾部时,大部分获得了受精能力。附睾头部的精子具有潜在的与透明带结合的能力,但结合位点或被遮盖,或未集中分布,没有与细胞内效应器形成功能统一体。在附睾内的运行过程中,精子表面的蛋白质发生了分布及结构变化,顶体素、前顶体素也发生了再加工和降解修饰。
近几年来研究发现,精子头后部具有透明质酸酶活性的膜蛋白PH-20,协助精子穿透卵丘细胞层。PH-20是一种单链蛋白质,通过糖基磷脂酰肌醇固定在精子膜上,该分子N端具有透明质酸酶活性。其透明质酸酶活性在协助精子穿透卵丘细胞过程中发挥重要作用。如果PH-20蛋白被透明质酸酶抑制剂和抗氨基端活性部位的抗体封闭,精子就无法穿过卵丘细胞层。PH-20能使顶体完整的精子穿透卵丘细胞层。虽然PH-20蛋白是在精子发生过程中形成,并分布于精子头部,但在附睾精子成熟过程中PH-20蛋白的定位发生了变化,主要定位于精子头后部质膜和顶体内膜,后者PH-20蛋白的量是前者的两倍,浓度明显增高。PH-20蛋白在精子膜上的重新分布和浓度变化在受精起始阶段有着十分重要的作用。 穿越卵丘细胞后所发生的精子对透明带的黏附和识别也十分重要。这种黏附和识别主要是精子表面的糖基和透明带的糖基结合蛋白ZP3之间的结合,该能力是在附睾中获得的。参与人精子透明带识别的有P34H蛋白等。P34H蛋白由附睾尾部上皮细胞分泌,定位于人精子顶体帽区,最初出现于附睾头部的精子,精子从附睾体到附睾尾的运行中该蛋白逐渐增多,射出的精子则很少,获能后又恢复,顶体反应后消失。P34H能够介导精子和透明带的结合。部分不育患者P34H水平低于正常人,其精子透明带结合率也明显下降。 在精卵结合过程中,存在于精子和次级卵母细胞上的蛋白质复合物有结合和融合作用,一些精子表面的蛋白在附睾内完成了再加工,有些附睾分泌的精子结合蛋白参与了精卵细胞膜融合过程),称作附睾内的精子成熟变化。
附睾是十分盘曲而细长的上皮管道。生精小管汇合形成睾丸网,进而形成输出小管,根据不同的物种,4到20个输出管腔汇聚成一个高度连续的管道——附睾管。在小鼠中附睾管长约1m,大鼠3m,人3~6m,而马有30m长。
在所有的哺乳动物中,附睾的每个区域进一步由疏松结缔组织隔膜分隔成小叶。这些小叶不仅对组织有支持功能,同时小叶间也形成了功能上的分离,使蛋白和基因在单个小叶上选择性表达,从而构成了小叶特异的特殊微环境。
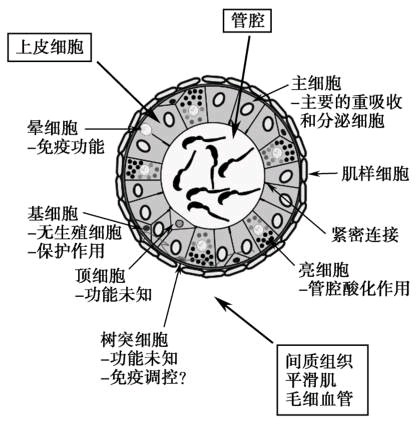
附睾中有几种上皮细胞类型,包括主细胞、顶细胞、狭窄细胞、亮细胞、基细胞、晕细胞和树状突细胞等。附睾各段的细胞分布是不同的,其中一些细胞分布在整个管腔,如主细胞,而其他细胞主要或特异分布在部分管腔,如狭窄细胞。这些上皮细胞有多种复杂功能,正是这些细胞的功能活动,构筑起了附睾精子成熟的微环境。
附睾精子成熟的概念是在20世纪20~30年代由Benoit和Young提出的。
不过在当时并没有引起明显的反响,并且在接下来的一段历史进程中总是存在两种不同的观点:一种观点认为附睾精子成熟仅是一种时间因素,即认为所谓附睾精子成熟变化是随着精子在附睾运行的时间推移而产生的,另一种观点则认为附睾精子成熟是一个复杂的生理过程,附睾精子成熟主要受到来自附睾微环境的影响,当然也有着精子本身因素的影响。
直到60年代Bedford和Orgebin Crist根据他们自己的实验再次明确提出附睾精子成熟的理论才得以重视,并在近20年期间附睾和附睾精子成熟的研究才有了较快的发展。
1992年在香港召开了第一次关于附睾研究的国际会议“epididymis and male fertility”,1998年在澳大利亚召开了第二次关于附睾研究的国际会议“the epididymis,cellular and molecular aspects”。这两次国际会议集中展示了附睾和附睾精子成熟研究的新进展,同时也把人们对附睾的认识推向深入。 针对附睾和附睾精子成熟的研究具有重要意义,完全阐明附睾精子成熟机制在生理上会产生重要影响,在此基础上,附睾源性男子不育症的诊断和治疗才有可能进一步发展。
三、附睾性精子异常
1、附睾性死精子症及精子变性
Leeanod在1988年观察到精子在附睾运行和贮存的过程中死亡和变性明显增加的病例,并提出了附睾死精子症和精子变性的病理假说。
附睾性死精子症和精子变性是附睾生殖病理的重要表现,也很可能是死精子症的重要原因。
附睾性死精子症和精子变性的主要特点包括:
①从睾丸活检的光镜和电镜观察发现睾丸精子是存活的,精子的细胞结构完整,无任何坏死和变性的病理表现;
②精子活动率甚低,一般低于10%,精子死亡率高,一般可超过40%~50%;
③增加射精频率,即缩短精子在附睾中的运行和贮存时间,能较明显提高精子的活动率和存活率。
推测附睾性死精子症和精子变性的可能主要原因包括:
①附睾的免疫功能是以血-附睾屏障和免疫屏障为特征的,正常情况下由生精小管的生精细胞和支持细胞形成血-附睾屏障;血-附睾屏障能有效阻止大分子(如精子抗原物质)漏出附睾腔外和阻止血清蛋白等漏入附睾腔内,以免发生自身免疫反应。当生殖系统有炎性感染或器官损伤(输精管结扎后),屏障遭到破坏,精子表面的特殊大分子物质与机体内的免疫系统相接触,就会发生精子抗原的自身免疫反应,引起抗精子自身抗体产生,体内产生一种免疫球蛋白抑制精子活力,而精子抗体与精子相互作用激活补体系统,在补体作用下,通过细胞毒性作用对精子细胞膜的通透性和完整性产生损伤,从而杀死精子。
②附睾上皮变性,导致附睾上皮大量溶酶体释放至管腔。
③附睾精子的死亡和变性,使精子胞质小滴和从顶体释放出来的溶酶体酶进一步损害还未变性和死亡的精子,促使其解体。
④活性氧由白细胞和精子产生并释放,一方面,活性氧是精子运动、获能、超激活运动、顶体反应、精卵识别所必需的,对维系精子正常功能起到重要作用;另一方面,由于病理、辐射、感染等各方面因素影响,精液中活性氧含量又会异常升高;精子膜脂质由于富含不饱和脂肪酸,细胞内几乎没有细胞质,抗氧化条件较差,在高反应能力的活性氧作用下,精子可能损伤,导致精子膜过氧化、核DNA片段化、蛋白变性等严重后果,对精子的存活和功能发挥造成巨大威胁。有文献表明,通过第一次射精后60分钟内进行第二次射精,可以改善具有附睾性死精子症男性的精子质量和存活力。在患有这种病症的男性中已经通过12小时间隔内频繁射精的方法来保证精子活力,强烈射精疗法的目的是减少到达附睾的“年轻”精子暴露于附睾不好环境的时间。对于死精子症患者,在短期约60分钟内第二次射精能产生与第一次射精相比质量更好的精液。在一项描述该方法的研究中,与基础精子数相比,在大多数情况下(70%)改善了第二次射精。其他人报道第二次精液中精子浓度没有统计学显著变化,但精子活力显著增加。
2、附睾梗阻性无精子症
附睾的主要功能之一是为附睾的精子成熟和精子贮存创造一个适宜的体液环境,附睾精子沉浸在一个液态的附睾微环境中。附睾的体液环境是通过调节附睾的分泌功能及吸收功能来实现的。
附睾分泌功能的缺陷和分泌障碍可导致在附睾管腔中形成一个脱水状态。附睾继续分泌高分子量糖蛋白但无正常液体分泌,使附睾管道阻塞,形成梗阻性无精子症,从而可导致男性不育。
梗阻性无精子症是由于输精管道的梗阻使精子的运输发生障碍而产生的无精子症。梗阻性无精子症在男性不育中的发生率约为1%。在无精子症患者中,梗阻性原因所占的比例较多,为42.4%~48%。附睾梗阻是梗阻性无精子症的最常见原因,在FSH低于正常值高限2倍的无精子症中占30%~67%。
先天性附睾梗阻常伴有先天性双侧输精管缺失(CBAVD),这些病例中82%至少有1个囊性纤维病基因点突变,这种病常伴有附睾远端部分缺如和精囊发育不良。先天性附睾梗阻还包括杨氏综合征(Young综合征),梗阻的原因主要是近端的附睾管腔内纤维化所致。有研究表明附睾的分泌功能是和附睾上皮氯离子通道密切相关。如果附睾上皮的氯离子通道及其调节发生障碍,就能导致附睾的分泌障碍,造成附睾管道内的脱水状态,引起黏稠性物质积聚,从而造成管道阻塞。
(一)囊性纤维化
囊性纤维化跨膜传导调节因子(CFTR)广泛表达于人体各种器官的上皮细胞中,包括气管,消化道和生殖道。编码CFTR的基因的突变引起囊性纤维化(CF),这是高加索人中最常见的致死性遗传疾病,每3500个新生儿中大约发生1例。CF患者在多器官中表现出系统性疾病,包括慢性肺部感染、炎症,胰腺功能不全和不育症,其中不育症的主要原因被认为是CFTR突变导致的电解质转运不良。CF的一个标志是男性不育,事实上,97%~98%的男性CF患者由于先天性双侧输精管缺失(CBAVD)而不育,导致梗阻性无精子症。除了CBAVD,在非阻塞性无精子症,少精子症,弱精子症和畸形精子症中也发现CFTR突变频率的增加。其临床表现多表现为进行性肺衰竭、胰腺功能不全及男性不育等。
CBAVD约占无精子症的15%~20%,近几年越来越多的研究显示该病与囊性纤维化(cystic fibrosis,CF)有关,并被公认为是CF的一种临床亚型。国外报道CBAVD患者的CFTR基因突变以ΔF508号外显子第1653~1655位三个碱基TTT缺失,导致第508位苯丙氨酸缺失最为常见,高达70%。国内对患者的基因突变情况研究较少,致病机制尚不明确。
CBAVD的发病机制可能与胚胎发育期CFTR基因突变有关,使Müller管异常,中肾管停止发育或缺陷,导致输精管发育畸形与缺失,且常伴有精囊腺缺如或纤维化。对原代啮齿动物Sertoli细胞和生殖细胞以及来自CFTR敲除小鼠或隐睾模型的睾丸的研究 结 果 表 明,CFTR通 过HCO3-/sAC/cAMP /CREB(CREM)途径参与精原细胞的NF-κB/COX-2/PGE2途径,实验还揭示了CFTR在精子获能中起到关键作用,直接或间接介导对于获能至关重要的HCO3-进入。CFTR在最新的研究中正在成为一个多功能的基因,介导各种生殖过程相关的不同信号通路,此外,其在电解质和流体转运中的作用是公认的,能调节雄性生殖道的管腔微环境。还有研究提示Y染色体的基因微缺失也与CBAVD有关,14例CBAVD的男性不育患者中发现2例存在AZFa位点的缺失。Daudin等报道CBAVD中24.5%的患者无突变,Mecallum等推测这些CBAVD患者的形成是由于在其胚胎发育早期(7周前)有一个非CFTR基因的突变,它导致整个中肾管异常发育从而形成CBAVD。另外在一些家系中父子同胞携带同一突变时仅其中之一患CBAVD,这说明在发生过程中除CFTR基因异常外,还可能存在其他遗传因素或环境因素的作用。各种因素如干扰中肾管的正常发育或退化,可导致绊状畸形发生。
对囊性纤维化无精子症患者不能精道重建,所以他们要生育唯一可选择的是辅助生殖技术,即采用显微外科技术从附睾(MESA)或直接从睾丸实质(TESE)获取精子用于随后的卵胞质内单精子注射(ICSI)。不推荐传统的IVF,因为其受孕率太低。
(二)杨氏综合征
1970年,利物浦泌尿科医师大卫·扬(David Young)观察到54%的患者有梗阻性无精子症并伴随有肺部缺陷,认为无精子症与肺部之间有关联,称作Berry-Perkins-Young综合征,简称为杨氏综合征。杨氏综合征是一种罕见的疾病,包括三种表现:梗阻性无精子症,支气管扩张和鼻窦炎,是一个公认的会造成男性不育的疾病。据报道杨氏综合征在男子不育症中占3.5%,在男子阻塞性不育症中约占21%~67%,多数报道约占50%。最近欧洲和美国的几个案例报告认为减少汞的使用可能使发病率下降,童年时期汞接触过多可能是病因之一。在杨氏综合征的相关统计中,汞中毒(粉红病)的概率在10%左右。汞能抑制含巯基的酶,与硫醇反应形成硫醇盐,而硫醇盐被认为能抑制糖酵解,阻碍机体必要的正常功能和获取能量供应精子和纤毛。
杨氏综合征的主要特点在于附睾上皮分泌液逐步减少,黏度增加,内容物黏厚,从而一步步导致附睾通道的梗阻,造成阻塞性无精子症。因此杨氏综合征导致的无精子症是渐进性的,可由完全畅通到不完全性阻塞直至完全性阻塞,表现在精子数量上从开始正常到减少直至精液中缺乏精子。在附睾渐进性梗阻过程中附睾的功能性指标也会发生相应的变化。此外,常伴有呼吸道感染。而呼吸道感染也可能是由于呼吸道黏液分泌异常,引起黏液浓缩的呼吸道清除功能下降,最终导致呼吸道感染。事实上由于此病发病机制尚不清楚及缺少相关的发病率资料,因此,尚不能确定是否杨氏综合征本身代表一个病种。目前对杨氏综合征还无良好的治疗方法。尝试外科学方法解除精道梗阻没有或仅有暂时效果。因此,采用显微外科技术从附睾(MESA)或直接从睾丸实质(TESE)获取精子用于卵胞质内单精子注射(ICSI),是希望生育的患者可选择的治疗方法。用附睾输精管吻合法虽能解决附睾的通道,但不能解决附睾的精子成熟。也可应用某些药物降低附睾分泌的黏稠性,关键问题应该解决附睾上皮氯离子通道及其调节,这样才能从根本上解决附睾阻塞性无精子症。
四、附睾与男性避育
随着附睾研究的进展及人们对附睾精子成熟认识的深化,学界已认识到附睾是男子抗生育中最理想的靶器官,是男子抗生育研究的主攻方向和战略要地,这也可以达成人们的期望——功能性不育,指不影响睾丸精子发生,不影响男子生殖内分泌功能,不影响性功能,仅干扰附睾精子成熟,从而使其失去生育能力。
五、附睾与中医“以通为用”治疗男性不育症
基于以上认识,附睾的通畅及功能的正常对于保持精子能力尤其重要,而精子能力与男性生育息息相关。中医以通为用,采用通法治疗男性不育症临床效果可观。