鼻咽癌是常见的头颈部恶性肿瘤,主要以低分化和未分化癌为主。据国际癌症研究机构(International Agency for Research on Cancer, IARC)统计,2020年全球年新增鼻咽癌患者约13万人,发病率2.4/10万人[1]。中国鼻咽癌发病率位居全球之首。2022年估计中国鼻咽癌新增患者达6.4万人,每年约3.6万人死亡。发病率4.3/10万人,死亡率2.4/10万人[2-3]。鼻咽癌起病隐匿,且具有早期转移的趋势。75%-90%的病例在诊断时存在淋巴结转移,5%-11%的患者在诊断时存在远处转移[4-6]。CSCO和NCCN指南推荐含铂化疗联合或不联合抗PD-1/PD-L1单抗作为复发转移性鼻咽癌患者的一线标准治疗,该一线标准治疗失败后,CSCO和NCCN指南推荐以卡培他滨等化疗药物为主的二线系统性治疗。前述一、二线系统治疗失败后的复发转移性鼻咽癌末线患者,国内外尚无具有循证学依据的标准治疗药物,临床上末线患者可接受医生选择的单药化疗药物的治疗,且其疗效较差。因此,临床上复发转移性鼻咽癌末线患者治疗中,存在巨大的未满足的临床治疗的需求。
临床试验
百利天恒正在开展一项在《既往经PD-1/PD-L1单抗治疗且经至少两线化疗(至少一线含铂)治疗失败的复发性或转移性鼻咽癌患者中对比BL-B01D1与医生选择的化疗方案(末线)III期随机对照临床研究》,这项研究已得到国家药品监督管理局的批准(药物临床试验批准通知书编号:2021LP01684)

试验药物简介
BL-B01D1是一款首创EGFR×HER3双特异性抗体偶联药物(ADC),由独家的双特异性抗体和“连接子-有效载荷”组成,其中包含稳定、可切割的连接子和拓扑异构酶I抑制剂。BL-B01D1在I期临床研究中表现了良好的安全性和耐受性,目前BL-B01D1在复发性或转移性鼻咽癌患者的III期临床研究正在进行中,有望为末线鼻咽癌患者治疗提供更有效的治疗方案。

主要入组标准
1.性别不限, ≥18 岁,经组织学或细胞学检查确诊的经PD-1/PD-L1单抗且经至少两线化疗(至少一线含铂)治疗失败的复发性或转移性鼻咽癌患者;
2.体力状况评分ECOG 0或1分;
3.未患或无间质性肺疾病(ILD)病史、无并发肺部疾病导致临床重度呼吸功能受损、无严重心脏功能异常、无严重心脏病史、自身免疫性疾病史、HIV、未接受过器官移植;

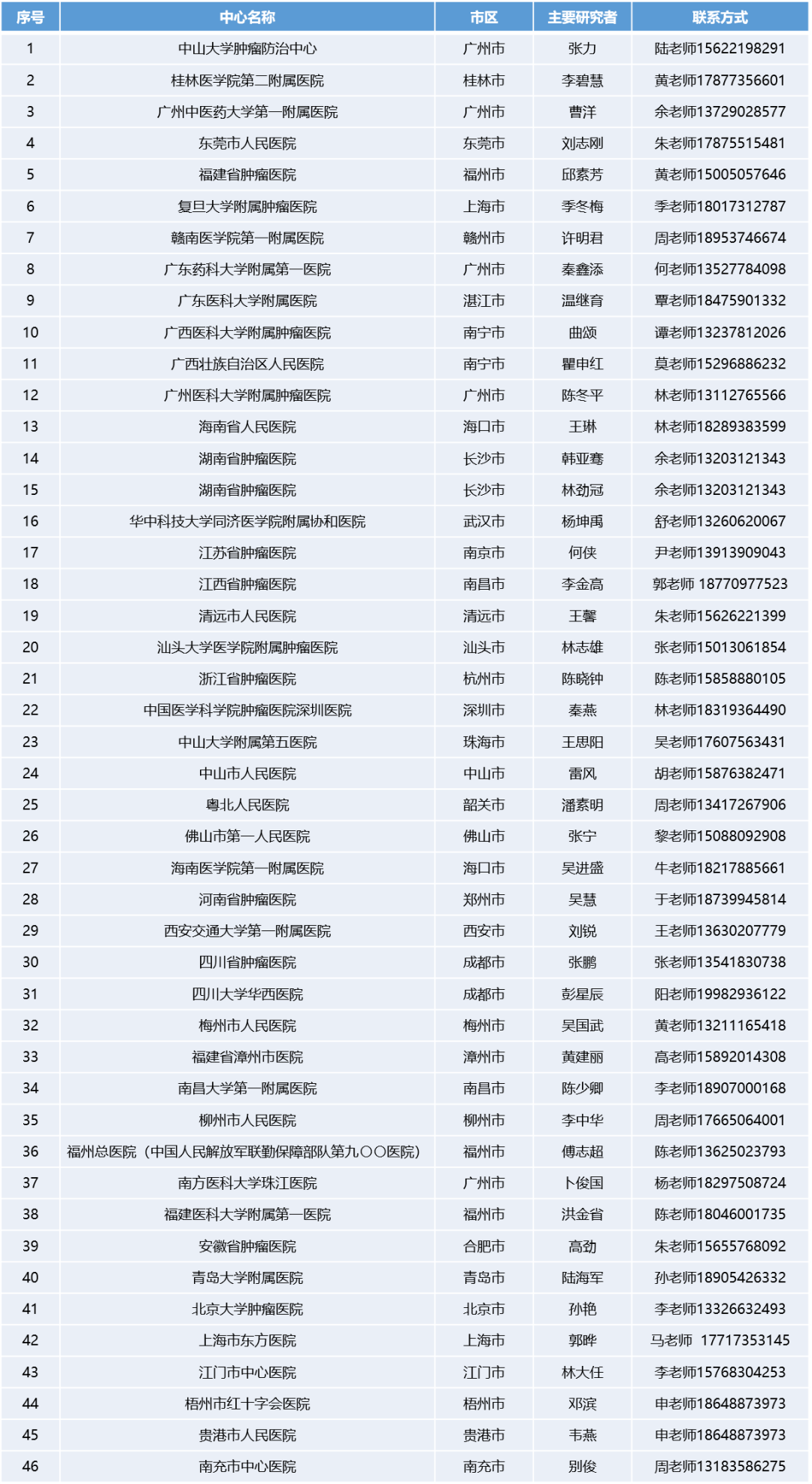
参研中心