
一、ADC后再换ADC是否可行?
ADC药物(抗体药物偶联物)的序贯使用是应对ADC耐药问题的一种新策略,已有多项研究表明ADC后再换ADC是可行的,但同时也可能出现交叉耐药,因此ADC药物使用顺序和序贯形式很重要。由于ADC耐药主要与ADC药物靶点识别、递送和载荷等因素相关,因此ADC药物序贯形式可大体分为3类:同靶点不同载荷序贯、不同靶点相同载荷序贯、不同靶点不同载荷序贯。
【交叉耐药】定义为在第一个ADC耐药后使用第二个ADC,于首次再分期时/前发生疾病进展(PD)。
部分实体瘤已上市ADC药物结构及适应症
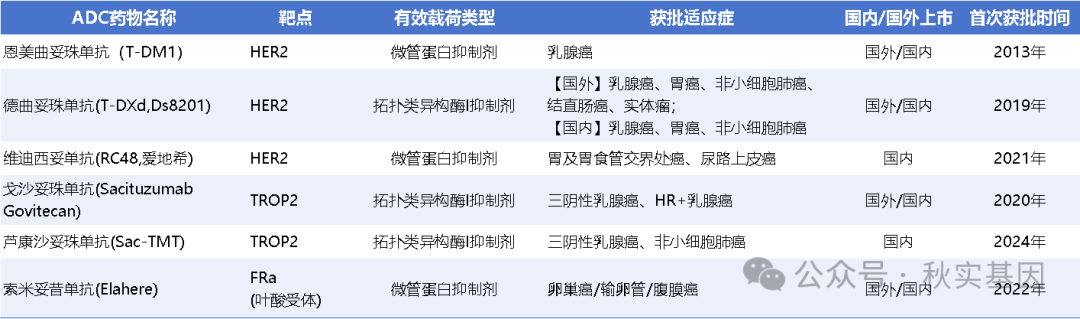
二、ADC药物序贯使用形式
1.同靶点、不同载荷ADC药物序贯
在同一靶点下,通过更换不同的载荷来克服耐药。例如,使用不同类型的载荷(如拓扑异构酶抑制剂和微管抑制剂)的ADC药物,由于它们的作用机制不同,可克服交叉耐药。如针对HER2阳性乳腺癌患者,可以先使用一款以拓扑异构酶抑制剂为载荷的ADC(如德曲妥珠单抗,T-DXd/Ds8201),如果耐药出现,可以换用以微管抑制剂为载荷的ADC(如恩美曲妥珠单抗,T-DM1)。
临床证据:
1)DESTINY-Breast02研究显示,T-DM1抗治疗后耐药的HER2阳性晚期乳腺癌患者再接受T-DXd治疗获益显著,与其他治疗组相比,中位无进展生存期(mPFS)达17.8个月 vs 6.9个月[1]。
2)DESTINY-Breast 03研究结果显示,针对HER2阳性乳腺癌患者,T-DXd治疗组与T-DM1治疗组比,中位无进展生存期(mPFS2)为40.5个月 vs. 25.7个月。其中T-DXd组后续有35.2%的患者接受了T-DM1单抗治疗,T-DM1组后续有17.3%的患者使用了T-DXd,证明了T-DXd治疗后再序贯使用T-DM1获益的可能性[2]。
2.不同靶点、相同载荷ADC药物序贯
针对不同的靶点,如TROP2和HER2,这些靶点可能在不同时间点共同存在于某些类型的肿瘤中(需检测靶点的表达),对应两个靶点的ADC 药物戈沙妥珠单抗(SG)和德曲妥珠单抗(T-DXd),载荷都是拓扑类异构酶抑制剂,可能序贯使用获益,但因仍可能存在交叉耐药,获益有限,不同研究数据也不太一样。
临床证据:
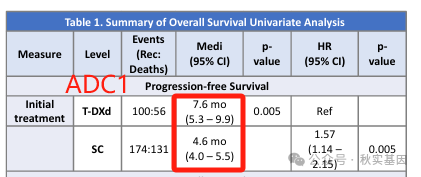
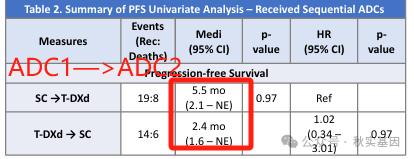
1)2023年一项真实世界研究发现,274例乳腺癌患者由33例使用ADC药物序贯治疗,HER2低表达晚期乳腺癌先用HER2靶点的ADC药物(T-DXd),再用TROP2靶点ADC药物(SG),ADC1 PFS和ADC2 PFS为7.6和2.4个月, 先用SG再用T-DXd的两个ADC PFS 为4.6和5.5个月[3]。
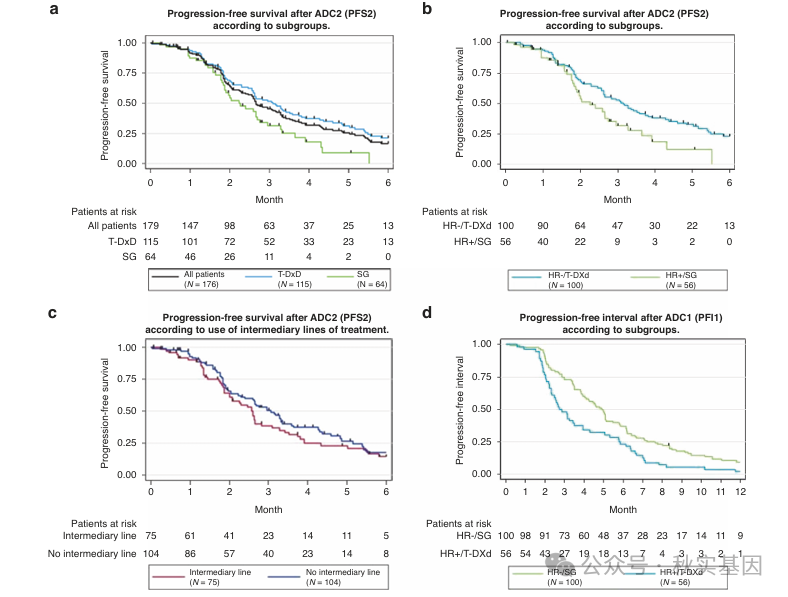
2)2024年ASCO大会报道了一项法国大型回顾性研究(ADC-LOW),评估了HER2低表达转移性乳腺癌患者序贯使用戈沙妥珠单抗(SG,靶向TROP2)和德曲妥珠单抗(T-DXd,靶向HER2)的疗效。结果显示:中位第二次无进展生存期(PFS2)仅为2.7个月,其中T-DXd作为ADC2序贯治疗时PFS2为3.1个月,SG为ADC2序贯治疗时PFS2为2.2个月。对于 SG 作为 ADC1 的 TNBC 患者和接受 T-DXd 作为 ADC1 的 HR+ 患者,中位 PFS2 分别为 3.2 个月和 2.3 个月。在 ADC1 和 ADC2 之间无中间治疗线的患者中,中位 PFS2 为 3.1 个月,而有中间治疗线的患者为 2.6 个月[4]。
3.不同靶点、不同载荷ADC药物序贯
如果两个ADC药物的靶点不同、载荷也不同,作用机制不同,可以双重克服交叉耐药。但需要确认同一肿瘤类型能同时符合两个不同靶点检出表达,且针对这两个靶点开发的ADC药物载荷也不同,如恩美曲妥珠单抗(T-DM1,靶向HER2)和戈沙妥珠单抗(SG,靶向TROP2),目前尚无此类大规模研究数据。
此外,一项关于乳腺癌ADC药物序贯使用的研究显示,共有193例者接受ADC治疗,其中32例HER2阴性或低表达患者接受了一个以上的ADC药物序贯治疗。第一个使用的ADC (ADC1)的中位PFS明显更长为7.55个月,而第二个ADC(ADC2)的中位PFS为2.53个月。靶点不同的ADC2患者PFS为3.25个月,而靶点相同的ADC2患者PFS为2.30个月。首次影像评估时,17例(53.1%)出现交叉耐药,12例(37.5%)无交叉耐药,3例无法评估。当序贯的两个ADC靶点相同时,9/13例(69.2%)出现交叉耐药,而当序贯的两个ADC靶点不同时,8/16例(50.0%)出现交叉耐药[5]。
三、结论
目前尚不能明确 ”相同靶点不同载荷ADC序贯“ 和 ” 不同靶点相同载荷序贯“ 哪个更有效,需要个体化区隔,更需要前瞻性大样本研究来确认最佳序贯形式和最佳用药顺序。
参考文献:
[1] André, Fabrice et al. “Trastuzumab deruxtecan versus treatment of physician's choice in patients with HER2-positive metastatic breast cancer (DESTINY-Breast02): a randomised, open-label, multicentre, phase 3 trial.”Lancet (London, England) vol. 401,10390 (2023): 1773-1785. doi:10.1016/S0140-6736(23)00725-0
[2] Sara A. Hurvitz, et al. “Trastuzumab deruxtecan versus trastuzumab emtansine in patients with HER2-positive metastatic breast cancer: Updated results of the randomized, phase 3 study DESTINY-Breast03.”2022 SABCS GS2-02.
[3]Akshara S. Raghavendra , et al. “Antibody-Drug Conjugates(ADCS)in EBreast Cancer: Real World Analysis of Outcomes.” 2023 SABCS PS08-01.
[4] Poumeaud F, Morisseau M, Cabel L, et al. Efficacy of administration sequence: Sacituzumab Govitecan and Trastuzumab Deruxtecan in HER2-low metastatic breast cancer. Br J Cancer.
[5]Rachel Occhiogrosso Abelman. “Sequential use of antibody-drug conjugate after antibody-drug conjugate for patients with metastatic breast cancer: ADC after ADC (A3) study.”2023 ASCO 1022P