
中华耳鼻咽喉头颈外科杂志编辑委员会鼻科组,中华医学会耳鼻咽喉头颈外科学分会鼻科学组
中华耳鼻咽喉头颈外科杂志 2019 年2月
前 言
慢性鼻窦炎(chronic rhinosinusitis,CRS)是耳鼻咽喉头颈外科的常见病,其病因学及病理生理机制复杂。近年来,我国CRS的诊疗和研究水平迅速提高,完成了多项较高等级循证医学证据的多中心临床研究,并完成了较大样本的全国流行病学调查,在 CRS发病机制研究、免疫病理学分类研究、组织病理学分型研究等领域已处于国际前沿水平。随着我国 CRS基础和临床研究的逐步深入,其诊疗策略也逐渐朝着更加符合中国人群 CRS病情特征的个体化和精准化方向发展。为此,中华耳鼻咽喉头颈外科杂志编辑委员会鼻科组联合中华医学会耳鼻咽喉头颈外科学分会鼻科学组,再次修订诊疗指南,以期更好地适应我国国情和临床需要,进一步提高我国CRS的诊断和治疗水平。
定义与分型
一、定义 CRS 是鼻窦黏膜的慢性炎性疾病,病程超过12周。
二、分型
1. 临床分型:CRS 在临床上可以分为两种类型:(1)慢 性 鼻 窦 炎 不 伴 鼻 息 肉(chronicrhinosinusitis without nasal polyps,CRSsNP);(2)慢性鼻窦炎伴有鼻息肉(chronic rhinosinusitis with nasal polyps,CRSwNP)。这是目前国际广泛采用的分型模式,简便实用。
2. 病理分型:CRS 根据炎性细胞浸润情况分为:(1)中性粒细胞浸润为主;(2)嗜酸粒细胞浸润为主;(3)淋巴细胞/浆细胞浸润为主;(4)混合型。也有文献报道将 CRS分为嗜酸粒细胞性和非嗜酸粒细胞性,但尚缺乏统一的分型参考标准,其临床应用还需要进一步探索。
流行病学
中国 7 个不同区域代表性城市多中心 CRS 流行病学调查数据表明,中国人群 CRS总体患病率为8%,略低于欧洲(10.9%)和美国(12%~14%)。流行病学研究表明,CRS 与变应性鼻炎(allergic rhinitis,AR)、哮喘及气道高反应的关系密切。CRS 患者中11.2%伴哮喘,27.3%伴气道高反应。在需手术治疗的CRS患者中,气道高反应的发生率为45.4%,哮喘的发生率为 10.4%,且嗅裂及上鼻道区域的息肉和息肉样黏膜水肿与气道高反应及哮喘的发生相关。
发病机制
CRS是一种高度异质性疾病,其发病与解剖结构、遗传及环境等多种因素有关。
一、发病相关因素
(一)解剖因素
窦口鼻道复合体解剖发育异常导致的通气和引流功能障碍可能促进了 CRS的发病,包括严重的鼻中隔高位偏曲压迫中鼻甲,过度发育的泡状中鼻甲、筛甲气房、Haller气房,以及鼻甲肥大、钩突移位或尾端肥大等。
(二)纤毛运动障碍
正常的纤毛功能对维持鼻腔和鼻窦的清洁具有重要作用。CRS纤毛功能异常多继发于炎症或原发性纤毛不动综合征。
(三)变态反应
变态反应可能不是引起 CRS的初始原因,但它是 CRS发生发展的一个易感因素,它可以加重 CRS患者黏膜的炎性反应。
(四)细菌
细菌是否为引起 CRS 的初始原因尚不明确。基于细菌 16S rRNA 的微生物组学研究提示,细菌菌群失衡可能与 CRS的发病、炎症状态及治疗效果有关。
(五)病毒
有研究显示,鼻病毒在 CRS患者中的分离率要显著高于健康对照人群,CRS患者对病毒先天性免疫的异常可能与嗜酸粒细胞性炎症有关。
(六)真菌
真菌在 CRS发病中的作用存在争议,目前多个前瞻性、随机双盲试验均未能证实抗真菌药物对CRS的治疗有效。
(七)超抗原
金黄色葡萄球菌肠毒素作为细菌超抗原,能够激活一系列免疫反应,诱导以 2 型 T 辅助细胞(type-2 T helper cell,Th2)反应为主的嗜酸粒细胞性炎症,但是该超抗原在中国人中的检出率较低。
(八)囊性纤维化
囊性纤维化是一种常染色体隐性遗传病,患者几乎全部合并 CRS,80%合并鼻息肉。患者鼻腔分泌物的黏稠度较正常人增加 30~60 倍,黏液纤毛清除系统的异常可引起鼻腔鼻窦反复严重感染。
(九)免疫缺陷
免疫缺陷是 CRS的易感因素,伴发免疫缺陷的患者 CRS复发次数多,同时可伴有其他系统的感染性疾病。
(十)阿司匹林耐受不良
中国人 CRS患者中阿司匹林耐受不良的发生率约为 0.57%。阿司匹林耐受不良患者若同时合并鼻息肉和哮喘,则称为阿司匹林三联症(aspirin triad)。阿司匹林耐受不良患者的鼻息肉范围广,易复发。
(十一)胃食管反流
胃食管反流患者比普通人群更易患 CRS,其可能的机制有:(1)胃酸直接刺激引起炎性反应和黏膜纤毛功能受损;(2)自主神经系统功能紊乱导致迷走神经功能增强,鼻窦黏膜肿胀堵塞窦口;(3)幽门螺杆菌的直接作用。
(十二)牙源性疾病
长入上颌窦的根尖炎症可以导致慢性上颌窦炎,致病菌多为厌氧菌。
(十三)医源性因素
不规范的鼻窦手术可造成窦口鼻道复合体粘连、黏膜大面积缺失或纤毛运动障碍。
(十四)遗传学因素
CRS有家族聚集倾向,CRSwNP遗传的可能性为 13.3%~52.0%,同卵双胞胎均发生鼻息肉的风险接近 100%。
二、免疫病理学特点
多种结构细胞、免疫细胞和炎性介质参与 CRS发病。
(一)CRSwNP的免疫病理学改变
CRSwNP 的组织病理学特征和浸润的炎性细胞类型具有人种和地区的差异,东亚地区(包括中国、韩国和日本)的 CRSwNP中约有 50%的患者表现为非嗜酸粒细胞性炎症,哮喘合并率较低。
中国人则可能与基质金属蛋白酶(matrix metalloproteinase,MMP)⁃7和 MMP⁃9的上调有关。
(二)CRSsNP的免疫病理学改变
CRSsNP的组织病理学表现主要为多种炎性细胞浸润、胶原沉积、黏液腺体增生和鳞状上皮化生,部分患者呈现明显的纤维化。中国人 CRSsNP 绝大多数表现为非嗜酸粒细胞性炎症。
诊 断
一、症状
1.主要症状:鼻塞,黏性或黏脓性鼻涕。
2.次要症状:头面部胀痛,嗅觉减退或丧失。
诊断时以上述两种或两种以上相关症状为依据,其中主要症状中的鼻塞、黏性或黏脓性鼻涕必具其一。
二、检查
1.鼻内镜检查:来源于中鼻道、嗅裂的黏性或黏脓性分泌物,鼻黏膜充血、水肿或有息肉。
2. 影像学检查:鼻窦 CT 扫描可显示窦口鼻道复合体和(或)鼻窦黏膜炎性病变。MRI对不同类型 CRS的鉴别诊断具有一定意义。
3.实验室检查:主要包括外周血、鼻腔分泌物和病理组织中的嗜酸粒细胞计数。目前具有临床可操作性和对预后判断有较明确意义的是外周血和病理组织中嗜酸粒细胞百分比,尤其是后者。有学者认为如果组织嗜酸粒细胞占总炎性细胞的百分比大于10%,则该组织表现为嗜酸粒细胞性炎症。诊断时依据临床症状、鼻内镜检查、鼻窦 CT扫描结果进行。在有条件的单位可以进行实验室检查,从而细化免疫病理学诊断分型。鼻窦 CT检查不能作为 CRS诊断的唯一依据。儿童 CRS诊断应以症状、鼻内镜检查为主,并严格掌握 CT 扫描指征。
三、病情评估
(一)主观病情评估
采用视觉模拟量表(visual analogue scale,VAS)进行评估。按照VAS评分将病情分为:轻度0~3 分;中度>3~7 分;重度 >7~10 分(图 2);若VAS>5分,则表示患者生活质量受到影响。也可采用鼻腔鼻窦结局测试20(sino⁃nasal outcome test⁃20,SNOT⁃20)量表进行评估。

(二)客观病情评估
1. 鼻腔和鼻窦解剖学变异的评估:
2. 感染和变应性因素的评估:鼻腔分泌物培养和药物敏感试验对治疗时抗菌药物的选择和病因的诊断有参考意义;对复发的 CRSwNP再次手术前,推荐对鼻分泌物涂片和(或)鼻黏膜/息肉病理组织进行嗜酸粒细胞检查。
3. CRS相关伴发疾病的评估:CRS常伴发局部或系统性疾病,包括腺样体增生、扁桃体肥大、哮喘及遗传性疾病等。需注意患者是否存在阿司匹林诱发哮喘的病史,以除外阿司匹林三联症。为防止手术中哮喘发作,对可疑伴哮喘的 CRS患者需行肺功能检查。
4. 嗅觉障碍的评估:CRS嗅觉障碍的发生率为61%~83%,目前应用较多的嗅觉心理物理测试方法包括 T&T嗅觉计测试、Sniffin′ Sticks嗅棒测试和宾夕法尼亚大学嗅觉识别测试。
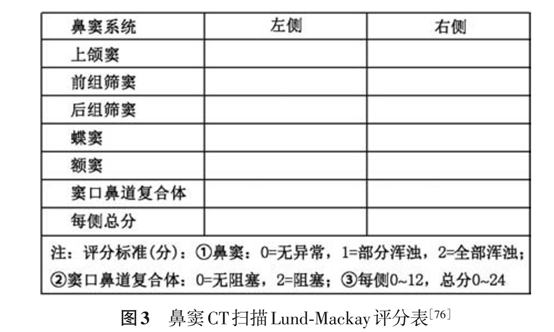
5. 病变范围的评估:作为评估病情严重程度的一项重要内容,推荐使用鼻窦CT扫描Lund⁃Mackay 评分法(图 3)。“海口标准”(1997)中的 CRSsNP(Ⅰ型)和 CRSwNP(Ⅱ型和Ⅲ型)也可作为对CRS分型和病变范围评估的一种方法。
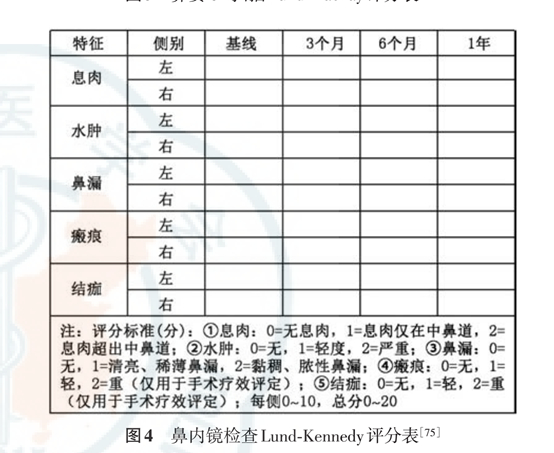
6. 鼻内镜检查量化评估:采用 Lund⁃Kennedy 评分法(图4)。

7. 鼻窦骨质变化的评估:CRS患者骨炎的发生率为33.83%~53.89%,CT上表现为骨质的增生性变化或骨质吸收。骨炎是导致难治性鼻窦炎(refractory chronic rhinosinusitis / difficult⁃to⁃treat rhinosinusitis)的一个重要原因,也是其持续性炎症的一个发源地,因此应重视鼻窦骨质变化的评估。但目前尚无简单易行的鼻窦骨质评估方法,推荐使用鼻窦整体骨炎评分系统(global osteitis scoring scale,GOSS,图5)。